Bize yazın: crohntedavisi@gmail.com
Madalyonun Ters Yüzü: Demir Eksikliği ve Kolorektal Kanser
|
Getting your Trinity Audio player ready...
|
İçindekiler
- 1 Özet
- 2 Tanıtım
- 3 Demir Eksikliği Tanımı
- 4 Demir Eksikliğinin Kanser Üzerindeki Etkileri
- 5 Kolorektal Kanser İlişkili Demir Eksikliği Anemisinin İnsan Klinik Çalışmalarından Elde Edilen Kanıtlar
- 6 Terapötik Bıçak Kenarında: Kolorektal Kanserli ve Demir Eksikliği/Anemisi Olan Hastalarda Demir Replasman Tedavisi
- 7 Çözüm
- 8 Yazar Katkıları
- 9 Çıkar çatışması
- 10 Teşekkür
- 11 Sözlük
- 12 Referanslar
Ayşegül Aksan , 1, 2, 3, † Karima Farrag , 3, 4, † Sami Aksan , 3, 4 Oliver Schroeder , 3, 4, † ve Jürgen Stein 2, 3, 4, *Yazar bilgileri Makale notları Telif hakkı ve Lisans bilgileri Sorumluluk Reddi
Özet
Anemili veya anemisiz demir eksikliği, kanserli bireylerde en sık görülen hematolojik bulgudur ve özellikle kolorektal kanserli hastalarda yaygındır. Demir, kanser biyolojisi ile yakından bağlantılı olduğu bulunan bağlamında birçok biyolojik işlevde önemli bir rol oynayan hayati bir mikro besindir. Bununla birlikte, bugüne kadar çok sayıda çalışma, aşırı demirin kanserin başlaması ve ilerlemesi üzerindeki etkilerini kapsamlı bir şekilde araştırmış ve gözden geçirmiş olsa da, demir eksikliğinin kanserle potansiyel ilişkisi büyük ölçüde ihmal edilmiştir ve iyi tanımlanmamıştır. Ortaya çıkan kanıtlar, azalan demir alımının ve düşük sistemik demir düzeylerinin kolorektal kanser patogenezi ile ilişkili olduğunu göstermektedir. Hem demir eksikliğini hem de fazla demiri önlemek için optimal demir alımının dikkatli bir şekilde dengelenmesi gerektiğini düşündürmektedir. Demir, immünolojik fonksiyonların sürdürülmesinde hayati olduğu için, yetersiz demir mevcudiyeti, neoplastik değişiklikler için immün gözetimi bozarak ve potansiyel olarak tümör immün mikro-ortamını değiştirerek onkojenisiteyi artırabilir. Klinik çalışmalardan elde edilen veriler, bu kavramları desteklemekte ve demir eksikliğinin kolorektal kanserli hastalarda daha düşük sonuçlar ve tedaviye yanıtın azalması ile ilişkili olduğunu göstermektedir. Burada demir eksikliğinin kanserle ilişkili etkilerini açıklıyoruz, demir eksikliğinin tümörijenez, kanser ilerlemesi ve tedavi yanıtındaki rolüne dair klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın. Demir, immünolojik fonksiyonların sürdürülmesinde hayati olduğu için, yetersiz demir mevcudiyeti, neoplastik değişiklikler için immün gözetimi bozarak ve potansiyel olarak tümör immün mikro-ortamını değiştirerek onkojenisiteyi artırabilir. Klinik çalışmalardan elde edilen veriler, bu kavramları desteklemekte ve demir eksikliğinin kolorektal kanserli hastalarda daha düşük sonuçlar ve tedaviye yanıtın azalması ile ilişkili olduğunu göstermektedir. Burada demir eksikliğinin kanserle ilişkili etkilerini açıklıyoruz, demir eksikliğinin tümörijenez, kanser ilerlemesi ve tedavi yanıtındaki rolüne dair klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın. Demir, immünolojik fonksiyonların sürdürülmesinde hayati olduğu için, yetersiz demir mevcudiyeti, neoplastik değişiklikler için immün gözetimi bozarak ve potansiyel olarak tümör immün mikro-ortamını değiştirerek onkojenisiteyi artırabilir. Klinik çalışmalardan elde edilen veriler, bu kavramları desteklemekte ve demir eksikliğinin kolorektal kanserli hastalarda daha düşük sonuçlar ve tedaviye yanıtın azalması ile ilişkili olduğunu göstermektedir. Burada demir eksikliğinin kanserle ilişkili etkilerini açıklıyoruz, demir eksikliğinin tümörijenez, kanser ilerlemesi ve tedavi yanıtındaki rolüne dair klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın. yetersiz demir mevcudiyeti, neoplastik değişiklikler için immün gözetimi bozarak ve potansiyel olarak tümör immün mikro-ortamını değiştirerek onkojenisiteyi artırabilir. Klinik çalışmalardan elde edilen veriler, bu kavramları desteklemekte ve demir eksikliğinin kolorektal kanserli hastalarda daha düşük sonuçlar ve tedaviye yanıtın azalması ile ilişkili olduğunu göstermektedir. Burada demir eksikliğinin kanserle ilişkili etkilerini açıklıyoruz, demir eksikliğinin tümörijenez, kanser ilerlemesi ve tedavi yanıtındaki rolüne dair klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın. yetersiz demir mevcudiyeti, neoplastik değişiklikler için immün gözetimi bozarak ve potansiyel olarak tümör immün mikro-ortamını değiştirerek onkojenisiteyi artırabilir. Klinik çalışmalardan elde edilen veriler, bu kavramları desteklemekte ve demir eksikliğinin kolorektal kanserli hastalarda daha düşük sonuçlar ve tedaviye yanıtın azalması ile ilişkili olduğunu göstermektedir. Burada demir eksikliğinin kanserle ilişkili etkilerini açıklıyoruz, demir eksikliğinin tümörijenez, kanser ilerlemesi ve tedavi yanıtındaki rolüne dair klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın. demir eksikliğinin kanserle ilişkili etkilerini açıklıyor, demir eksikliğinin tümör oluşumu, kanserin ilerlemesi ve tedavi yanıtındaki rolüne ilişkin klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın. demir eksikliğinin kanserle ilişkili etkilerini açıklıyor, demir eksikliğinin tümör oluşumu, kanserin ilerlemesi ve tedavi yanıtındaki rolüne ilişkin klinik öncesi ve klinik kanıtları inceliyoruz. ve bu sonuçları sınırlamak için yeterli demir takviyesinin önemini vurgulayın.Anahtar Kelimeler: demir eksikliği, demir eksikliği anemisi, kolorektal kanser, immün konak savunması, intravenöz demir tedavisiGit:
Tanıtım
Kolorektal kanser (CRC), dünya çapında en ölümcül üçüncü ve en çok teşhis edilen dördüncü kanserdir ve insidansı gelişmekte olan ülkelerde giderek artmaktadır ( 1 ). Hem genetik özellikler hem de çevresel faktörler bağırsak karsinogenezinde rol oynar ( 2 , 3 ). Diğer iyi bilinen katkıda bulunanların yanı sıra, demir son zamanlarda kolorektal kanserojenitede olası bir suçlu olarak ortaya çıkmıştır ( 4 ). Yayınlanmış veriler fazla oral demir alımı CRC (riski ile ilişkili olduğu hipotezini desteklemektedir 5 – 8 ).
Demir, kanser biyolojisi ile yakından bağlantılı olduğu bulunan birçok biyolojik fonksiyonda önemli bir role sahip olan hayati bir mikro besindir ( 4 , 9 , 10 ). İz element, enerji üretimi ve REDOX aracılı enzimler için bir katalizör olarak ara metabolik eylemler için gereklidir. Proteinler (demir doğrudan bağlanan veya heme veya demir-sülfür kümeler şeklinde demir ihtiva edebilir 11). Demir, sırayla demir kaynaklı apoptoza veya ferroptoza neden olabilecek serbest oksijen radikalleri üretir. Ayrıca, bu demir-oksijen kompleksleri, mutajeniteyi ve habis dönüşümü teşvik etmede suç ortağıdır. Dönüşüme uğrayan habis hücreler çoğalmak için büyük miktarlarda demire ihtiyaç duyarlar. Demir ayrıca, bağışıklık hücreleri tarafından yürütülen tümör gözetimi de dahil olmak üzere, bağışıklık fonksiyonlarının önemli bir aracısıdır ( 9 ). Konak savunmasının önemli bir yönü olan makrofajlarda sitokin üretimi, demir içeriği tarafından düzenlenir ( 11).). İdeal demir alımı, bu nedenle, demir eksikliği ve demir fazlalığı arasında dikkatli bir şekilde dengelenmelidir, çünkü her ikisinin de kanser gelişimi açısından potansiyel olarak önemli klinik sonuçları olabilir. Bununla birlikte bugüne kadar, çok sayıda çalışma kapsamlı bir şekilde aşırı demirin kanser başlangıcı ve ilerlemesindeki rolünü araştırmış ve gözden geçirmiş olsa da ( 5 , 9 , 10 , 12 – 14 ), demir eksikliğinin potansiyel olarak tümörijenik etkileri büyük ölçüde ihmal edilmiştir ve bunlar büyük ölçüde ihmal edilmiştir. henüz iyi tanımlanmadı ( 4 ). Bu, kesinlikle daha fazla araştırmayı hak ediyor, çünkü demir eksikliği özellikle KRK’li hastalarda hem tanı anında hem de hastalık süresi boyunca sıklıkla ortaya çıkıyor ( 15).– 17 ).
Aşırı demir alımının etkileri, CRC’nin hem etiyolojisini hem de prognozunu potansiyel olarak etkileyebiliyorsa, demir eksikliğinin fizyolojik etkileri de olabilir ( 18 – 20 ). Demir eksikliği anemisi (DEA) olan hastalarda KRK riskinin önemli ölçüde yüksek olduğu bulunmuştur ( 15 , 16 , 21 ). Ayrıca, demir eksikliği, kanserli hastalarda daha kısa sağkalım süreleri ile açıkça ilişkilidir ( 19 ). Bu bulgular şaşırtıcı değildir, çünkü demir eksikliği, bağışıklık hücresi üretimi için bir ön koşul olan hematopoezi sınırlayabilir ve bağışıklık hücrelerinin doğru çalışması için demir gereklidir ( 22 , 23 ).). Bu nedenle, kanser hastalarında demir eksikliği azalmış bir immün yanıtı elde edebilir, sonuç olarak, bir bozulmuş tedavi yanıtı, bir zayıf prognoz ve indirgenmiş genel sağkalım ( 18 – 20 ). Bu derlemede, demir eksikliğinin kanserdeki rolüyle ilgili madalyonun diğer yüzünü araştırıyoruz, demir eksikliğinin özellikle CRC’de tümör gelişimi ve ilerlemesi için anahtar olan bağışıklık fonksiyonları üzerindeki sonuçlarını ele alıyor ve bu sonuçları sınırlamak için mevcut demir tedavisi seçeneklerini açıklıyoruz.Git:
Demir Eksikliği Tanımı
Anemili veya anemisiz demir eksikliği kanserli bireylerde en sık görülen hematolojik bulgudur ve hastaların %40’ından fazlasında görülür. CRC’li hastalarda bildirilen oran daha da yüksektir, yaklaşık %60’tır ( 17 , 24 , 25 ). Kanserli hastalarda demir eksikliğinin iki formu gözlenebilir: mutlak demir eksikliği (AID) ve fonksiyonel demir eksikliği (FID).
AID, tükenmiş demir depoları ve yetersiz demir arzı ile karakterize edilirken, FID’de demir depoları yeterlidir, ancak eritropoez ve diğer demire bağımlı yollar için yetersiz demir arzı vardır ( 26 , 27 ). Kanserde FID’nin ana nedeni, interlökin (IL)-6, IL-1, TNF-a ve IFN-y gibi kanserle ilişkili proinflamatuar sitokinlerin salınımıdır. Bu sitokinler, hepsidin sentezini yukarı regüle ederek dolaşıma salınan demir miktarını azaltır ( 27 – 29 ). FID, eritropoezi uyarıcı ajanlarla (ESA) tedavi altında kemo ve/veya radyoterapinin neden olduğu miyelosupresyon veya artan eritropoez nedeniyle de gelişebilir ( 27 , 29 )). Kanser hastalarında sık görülen bir komorbidite olan kronik böbrek hastalığı, eritropoezi azaltarak ve hepsidin düzeylerini artırarak FID’ye neden olabilir ( 30 , 31 ). FID, bu bağlamda kanser anemisi veya kanserle ilişkili anemi olarak da bilinen, kronik hastalık anemisine (ACD) en büyük katkıda bulunanlardan biridir ( 29 , 32 ).
AID’de ise demir depoları gerçekten tükenmiştir. Beslenme eksiklikleri (örneğin, malabsorbsiyon, tümör kaynaklı anoreksi, yetersiz beslenme) ve özellikle CRC’de nadir olmayan açık veya gizli kan kaybı AID’ye katkıda bulunur ( 26 , 27 , 29 ).
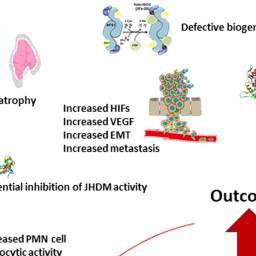
Şekil 1 kanserli hastalarda demir eksikliği ve aneminin sonuçlarına genel bir bakış sunar.

Kanserli hastalarda demir eksikliği ve aneminin sonuçlarına genel bakış.
Klinik Görüş: Kanserli Hastalarda Demir Eksikliği Teşhisi
Kanserli hastalarda demir eksikliğinin spesifik etiyolojisi tedavi yaklaşımının önemli bir belirleyicisi olduğundan, AID ve FID arasındaki ayrım esastır ( 26 , 27 , 33 , 34 ).
Perls’in Prusya mavisi boyaması ile kemik iliğindeki demir arzının analizi, demir eksikliği teşhisi için “altın standart”tır ( 35 ). Bununla birlikte, bu teknik maliyetlidir, oldukça invazivdir ve otomatik değildir, bunun bir sonucu olarak rutin uygulamada büyük ölçüde uygulanamaz.
Sağlıklı bireylerde, serum ferritin (SF) demir depolarının bir belirteci olarak kabul edilirken, transferrin satürasyonu (TSAT), ortalama alyuvar hacmi (MCV), hipokromik eritrosit yüzdesi (%HYPO), retikülositlerin Hb içeriği gibi diğer parametreler (CHr), çözünür transferrin (sTfR), kırmızı kan hücreleri (RBC’ler) ve çinko protoporfirin (ZnPP), biyolojik olarak mevcut demir miktarını yansıtır ( 26 , 27 ). Ancak bu parametrelerin çoğu kanserli hastalarda değişmektedir. Bu nedenle, bu ortamda demir eksikliği türlerinin farklılaşması birçok zorluğu beraberinde getirir ( 27 ).
Demir eksikliği, transferrin doygunluğu (TSAT) < %20 olarak tanımlanır ve ayrıca AID (SF < 100 ng/mL) veya FID (SF > 100 ng/mL) olarak da karakterize edilebilir ( 27 , 33 , 34 ). SF, kansere bağlı inflamasyonun varlığı nedeniyle bir akut faz proteini gibi davrandığından, kanserli hastalarda kesme noktası, inflamatuar hastalığı olmayan kişilere göre daha yüksektir (ikincisinde SF için cut-off 30 ng/ mL) ( 34 ). Daha yerleşik belirteçler TSAT ve SF’ye ek olarak, ZnPP, AID’de arttığı bulunduğundan ayırıcı tanıya değerli bir katkı sağlayabilir ( 34 , 36 , 37). Çözünebilir transferrin reseptörü (sTfR) seviyelerinin de AID’de arttığı ve FID’de azaldığı bildirilmiş olsa da ( 27 , 32 ), seviyeleri kemoterapiyi takiben düşebilir ve ESA tedavisinden sonra artabilir. Bu nedenle, sTfR ve sTfR/log ferritin indeksi gibi sTfR ile ilgili belirteçler, onkolojik bir ortamda belirteçler olarak daha az uygundur ( 32 , 34 , 37 ). CHr, %HYPO, MCV ve RBC’ler dahil olmak üzere diğer demir eksikliği belirteçleri, AID ve FID arasında ayrım yapamaz ( 34 ).
Dolaşımdaki hepsidin ölçümü, yalnızca demir durumunu değerlendirmede değil, aynı zamanda demir tedavisine yanıtı tahmin etmede de ek fayda sağlayabilir ( 38 , 39 ). Ancak henüz, hepsidin için onaylanmış bir klinik sınır değer veya klinik uygulamada tam olarak kullanılmasına izin verecek basit bir standart test yoktur ( 27 , 38 ).Git:
Demir Eksikliğinin Kanser Üzerindeki Etkileri
Demir, anti-inflamatuar ve antioksidan özelliklere sahiptir ve bağışıklık sisteminin işlevlerinde hayati bir rol oynar ( 4 , 20 , 40 ). Aynı zamanda, hücre proliferasyonu ve farklılaşması, bağırsak sağlığı, DNA sentezi ve onarım bakım ve ilaç ve toksinler (metabolik parçalanması gibi birçok temel fizyolojik işlemlerde, vazgeçilmez bir rol oynar 41 – 43 ). Demir homeostazı ( 23 , 44 , 45 ) ve demirin kanserin başlaması, ilerlemesi ve tedavisindeki rolü çok sayıda yayında kapsamlı bir şekilde gözden geçirilmiştir ( 9 , 10 , 12, 13 , 46 ). Bu bölümde, özellikle temel bilimden klinik sonuçlara kadar demir eksikliğinin CRC üzerindeki etkilerine odaklanıyoruz (Şekil 1).
Demir Eksikliği ve Kanser Epigenetiği
Epigenetik mekanizmalar başlatılması ve kanserin ilerlemesinde (çeşitli ve önemli roller oynadığı önemli aktörler olarak ortaya çıkmıştır 47 – 49 ). Demirin epigenetikteki rolü tanımlanmış olsa da, altta yatan mekanizmalar henüz tam olarak aydınlatılamamıştır. Demir, vücudun her hücresinde demir-kükürt (Fe-S) küme sentezi için gereklidir ( 50 ) ve DNA duplikasyonu, onarımı ve epigenetiğinin anahtar enzimlerinin prostetik gruplar olarak Fe-S kümelerine sahip olduğu bilinmektedir ( 50 – 54 ). Demir eksikliği, Fe-S kümelerinin kusurlu biyogenezine neden olarak DNA replikasyon stresini ve genom kararsızlığını indükler ve bunların her ikisi de malign transformasyonun göstergesidir ( 20 , 54).
Jumonji-C (JmjC) alanı içeren histon demetilazlar (JHDM’ler), translasyon sonrası değişikliklerin en yaygın bölgeleri olan histon kuyruklarının lizin kalıntılarını demetile ederek gen ekspresyonunu etkiler. JHDM’lerde genetik değişiklikler çeşitli insan kanserlerinde rapor edilmiştir ( 55 – 57 ). Sonuç olarak, JHDM’lerin onkogenezde yer aldığına inanılmaktadır ( 55 ). JHDM’ler, kofaktör olarak demire sahip demire bağımlı enzimlerdir ( 51 , 57 ). Bu nedenle, demir eksikliği, olası onkolojik olarak ilgili etkilerle birlikte JHDM’lerin aktivitesini inhibe edebilir. Ayrıca, demir eksikliğinin ortak bir özelliği olan hipoksinin de JHDM aktivitesinde bir kayıpla sonuçlandığı ve muhtemelen kemokin ekspresyonundaki değişikliklere katkıda bulunduğu bulunmuştur ( 56).). JHDM’lerin rolü, kanser tipine bağlı olarak iki yönlü olabilir. Genel olarak, bu nedenle, optimal demir seviyelerini korumak önemlidir ( 55 ).
Kodlamayan RNA ailesinin üyeleri olan mikroRNA’ların (miRNA’lar), tümörlerin başlaması, ilerlemesi, metastazı ve istilacı aktivitesindeki rolü, geçtiğimiz on yılda karakterize edilmiştir. miRNA’lar, ökaryotik genomik DNA tarafından kodlanan, evrimsel olarak korunmuş, endojen, tek sarmallı, 18-22 nükleotid uzunluğunda küçük RNA’lardır. MiRNA’ların anormal ekspresyonu, onkogenler ve tümör baskılayıcı genler dahil olmak üzere çeşitli genlerin normal ekspresyonunu değiştirebilir ( 47 , 58 ). Nihayetinde, miRNA ekspresyonunun ve ilgili biyolojik süreçlerin düzensizliği, kanserin ilerlemesi ve gelişmesi açısından kötü sonuçlara ve ayrıca daha zayıf terapötik yanıta yol açar ( 58 – 60). Ek olarak, miRNA’ların ~%50’si, genomik kanserle ilişkili heterozigotluk kaybı veya amplifikasyon kaybı bölgelerinde ve kromozomlar içindeki kırılgan bölgelerde bulunur ve bu, miRNA’ların tümörijenezdeki önemli rolünün altını çizer ( 61 ).
Demir eksikliği arızalı heme biyosentezini ve bozulmasını, hipoksi yol açarak MiRNA oluşum ve ifade ve alter MiRNA aracılı gen regülasyonu ağları etkilediği düşünülen ve ROS (arttırılır 62 – 66 ). Bu nedenle, demir eksikliği ayrıca tümör oluşumu riskini artırabilir ve miRNA’ların gen düzenleme sistemini olumsuz etkileyerek kötü kanser prognozuna ve kötü terapötik sonuçlara yol açabilir ( 67 ).
Demir eksikliğinin ortak bir özelliği olan hipoksinin, hipoksi ile indüklenebilir faktörün (HIF) ana düzenleyicisi olan von Hippel-Lindau (VHL) genini bozarak farelerde tümörün ilerlemesinde ve tedavi direncinde önemli bir rol oynadığı gösterilmiştir. bir tümör baskılayıcı ( 68 ). Demir eksikliği olan, bağışıklığı yetersiz fare ksenograft modellerinde, Notch sinyal yolunun bozulduğu ve transkripsiyon faktörü Snail’in ifadesinin yükseldiği gösterildi ( 69). Salyangoz, tümör büyümesi, metastaz ve tedavi direnci ile ilgili sayısız etkiye sahiptir: Artan ekspresyonu, epitelyal-mezenkimal geçişi değiştirerek (epitel baskılayarak ve mezenkimal belirteçleri güçlendirerek) hücre hareketliliğini ve istilacılığı destekler. Ayrıca, Salyangoz, tümör hücrelerinde kök hücre benzeri özellikler sağlayarak terapi direncini arttırır ( 70 ).
Demir eksikliği, hipoksi yoluyla, mitokondri aracılı hücre ölümünü engelleyen protein kodlayan gen olan BCL2L1’in artan ekspresyonu ile ilişkilendirilmiştir. Ayrıca, demir eksikliğinin sadece malignite ve inflamasyon ile ilişkilendirilen sistein proteaz katepsin Z geni olan CTSZ’nin değil, aynı zamanda dahil olan sistein peptidi Kaspaz 5 geni olan CASP5’in ekspresyonunu da engellediği gösterilmiştir. hücresel apoptozda ( 71 ).
Bu nedenle demir eksikliği, muhtemelen onkogenez ile ilişkili olan çeşitli epigenetik değişiklikler ve epigenetik mekanizmalarla ilişkilidir. Bununla birlikte, kanser gelişimi ve ilerlemesindeki rolleri tam olarak aydınlatılmamıştır.
Demir Eksikliği ve Prooksidan ve Antioksidan Aktiviteler
Demir eksikliğinin pro- ve antioksidan sistemlerde (REDOX) bir dengesizliğe neden olabileceği öne sürülmüştür ( 20 ). Demir eksikliği olduğunda, katalaz (CAT), süperoksit dismutaz (SOD), glutatyon peroksidaz (GSH-Px) ve A, C ve E vitaminleri gibi hem enzimatik hem de enzimatik olmayan antioksidan sistemlerin seviyesinin olduğu bulunmuştur. azaldı ( 6 , 72 – 74 ). Öte yandan Cu ve Zn-SOD gibi oksidatif stres belirteçleri artar ( 20 , 75 ). Bu değişiklikler, vücudun toplam antioksidan kapasitesinde bir azalma ile birlikte artan reaktif oksijen türlerinin (ROS) oluşumuna yol açar ( 74 , 76 – 78). ROS, farklı hedeflere karşı değişen reaktiviteler sergilerken, proteinleri, lipidleri ve DNA’yı oksitleyerek hücrelere zarar verme yeteneğini paylaşırlar. ROS’un hücre hasarına ve DNA mutasyonuna neden olma potansiyeli, zamanla biriken ROS hasarının bir yansıması olarak tümör hücresi gelişimi, metastaz, tümör agresifliği ve tedavi direnci ile doğrudan veya dolaylı olarak ilişkili olabileceğini düşündürmektedir ( 20 , 79 , 80 ).
Demir eksikliğinin oksidatif stresi artırarak mitokondriye zarar vererek mitokondriyal DNA’yı bozabileceği gösterilmiştir ( 81 ). Mitokondri, öncelikle oksidatif fosforilasyondan, oksijen ve besinlerden hücre içi enerjinin üretilmesinden ve ayrıca hem sentezinden ( 82 ) ve ökaryotik demir-kükürt (Fe-S) protein kümelerinin birleştirilmesinden ( 83 ) sorumlu olan hücre organelleridir . Mitokondri ayrıca otoreprodüksiyondan sorumludur. Mitokondriyal fonksiyonların bozulması bu nedenle nükleer genomun bütünlüğünü bozabilir ( 84 ).
Hemoproteinler, protein olmayan bir bileşen veya heme (veya bunun bir türevi) adı verilen prostetik grup içeren çeşitli yapılara ve işlevlere sahip konjuge proteinlerdir. Oksidatif stres nedeniyle artan ROS, hemoproteinlerin bu hem gruplarını boşaltmasını indükleyebilir, bu da serbest radikallerin ek üretimini tetikleyebilen dolaşımdaki serbest heme neden olabilir. Hem oksijenaz-1 geninin (HMOX1) transkripsiyonunun hızlı indüksiyonu hem de hızlı katabolizma oluşturan heme oksijenaz-1 (HO-1) izoenzim protein ekspresyonu gibi serbest heme’nin pro-oksidan etkilerini önleyebilen bir dizi mekanizma vardır. ortaya çıkan hücre hasarını sınırlamak için serbest heme ( 85 , 86). HO-1, hücresel homeostazda yer almanın yanı sıra, oksidatif doku hasarını önlemede ve hücre içi inflamatuar mekanizmalara, apoptoz ve hücre proliferasyonuna aracılık etmede önemli bir rol oynar ( 85 ). Lai et al. ( 87 ), yeterli demir olmadan, HCT-116 insan kolon adenokarsinom hücrelerinin, toksisiteye yanıt olarak HO-1 genini tamamen ifade edemediğini bildirdi. Demir, HO-1 gen ekspresyonu için gerekli olduğundan, demir eksikliği HO-1 ekspresyonu yoluyla sitoproteksiyonun azalmasına neden olabilir ( 20 ).
Heme, CYP (bağırsak sitokrom P450) antioksidan enzim sisteminin ( 88 – 90 ) ayrılmaz bir parçasıdır . Demir eksikliğinin bağırsak hücrelerinde CYP sistem aktivitesini azalttığı gösterilmiştir. Hem bir ksenograft fare modelinde hem de CRC hücrelerinde, kolorektal karsinojenezi teşvik etmek için CYP2S1 gen tükenmesi tanımlandı ( 91 – 93 ). Bu nedenle, demir eksikliğinin hem sentezi üzerindeki etkileri, CYP sistemine müdahale ederek CRC için bir risk faktörü oluşturabilir.
İnsan beyin hücrelerinde yapılan in vitro çalışmalar, demir eksikliğinin hem içeren elektron taşıma proteininin (sitokrom-c oksidaz/kompleks IV) önemli ölçüde azalmasıyla sonuçlandığını göstermiştir ( 94 ). Bunun hem metabolizmasında bozulmaya, oksidatif streste artışa ve mitokondriyal disfonksiyona neden olduğu gösterilmiştir ( 94 ). Bunların hepsi kanserin karakteristik belirtileridir ( 20 , 95 ).
Transkripsiyon faktörü Nrf2 (nükleer faktör-E2 ile ilgili faktör-2) oksidatif stres için hücresel bir sensör olarak işlev görür. Nrf2 aktivasyonu yoluyla faz II proteinlerinin genetik transkripsiyonu, muhtemelen vücudun oksidatif stres ve toksinlere karşı bağışıklık tepkisi için en önemli sinyal yolunu temsil eder. Nrf2 bu nedenle hücre korumasında önemli bir rol oynar. Demir eksikliğinin oksidatif stres için otofajiyi ve Nrf2 sinyalini aktive ettiği bulunmuştur ( 96 ). Nrf2 aktivasyonu kanserle ilişkilendirilmiştir ve küçük hücreli olmayan akciğer kanseri gibi tümör tiplerinde kötü sonuç ve azalmış sağkalım ile ilişkilidir ( 97 , 98 ). Nrf2’nin yapıcı aktivasyonunun onkogenezi teşvik edebileceği öne sürülmüştür ( 99 , 100) anjiyogenezi, metabolik yeniden programlamayı, kronik proliferasyonu ve hücre ölümüne karşı direnci teşvik eden eylemler yoluyla ( 101 , 102 ). Bu nedenle, demir eksikliği, oksidatif stres için otografi ve Nrf2 sinyalini aktive ederek onkogenezi teşvik edebilir.
Demir Eksikliği, Bağışıklık Tepkisi ve Hücre Fonksiyonu
Demir homeostazının hücresel bağışıklık tepkileri ile etkileşimi karmaşıktır ve bağlama bağlıdır. Demir eksikliği nedeniyle hücresel bağışıklığın ve bağışıklık hücrelerinin antimikrobiyal aktivitelerinin bozulması, habis dönüşüm potansiyelini belirlemesi ve ortadan kaldırması gereken bağışıklık sisteminin bağışıklık gözetim mekanizmalarına uygun olmayan bir mikro-ortam oluşturabilir. Ayrıca, modifiye edilmiş tümör mikro-ortamı içinde, bağışıklık hücrelerinin kendileri bir pro-tümörijenik tepki gösterebilir ( 4 , 14 , 20 , 85 ).
Nükleer faktör (NF-κB) ve hipoksi ile indüklenebilir faktörler (HIF’ler), bağışıklık sistemi regülasyonu için kritik olan transkripsiyon faktörleridir ( 103 ). Tümör hücrelerinin fizyolojisi, onların hızla büyümesine ve çoğalmasına ve apoptozdan kaçınmasına izin verir. Ayrıca bu hücrelerin özelliği, büyümeyi inhibe eden sinyalleri yok sayma, anjiyogenezi, doku istilasını ve metastazı başlatma ve sonsuza kadar çoğalma kapasiteleridir. Bu süreçlerin aracılığında yer alan genlerin neredeyse tamamı NF-κB transkripsiyonu ile düzenlenir ( 104 ). Düşük hücre içi demir seviyeleri, NF-κB gen ailesinin bir alt birimi olan Re1A’nın fosforilasyonunu açıkça azaltır ve HIF’lerin prolil hidroksilasyonunu bozar ( 71 , 105 ). Kendi başına demir eksikliğive demir eksikliğinin neden olduğu hipoksi, anjiyogenez ve tümör hücrelerinin metabolik yeniden programlanması ile ilişkili hedef genleri yukarı regüle ederek kanserin ilerlemesine aracılık ettiği bilinen HIF’lerin aktivasyonunu tetikleyebilir ( 106 , 107 ) ve böylece kemo ve radyoterapilere karşı dirence neden olabilir ( 108 , 109 ). HIF-la, katı tümörlerin büyümesinde, ilerlemesinde ve metastazında anahtar bir rol oynar ( 110 , 111 ). Demir eksikliğinin HIF-1 transkripsiyonunu desteklediği ve HIF-2 transkripsiyonunu inhibe ettiği, böylece HIF’ler ve NF-KB arasındaki sinerjik sinyal yollarını bozduğu bulunmuştur ( 71). Sonuç olarak, demir eksikliği bağışıklık tepkisini zayıflatabilir, hem onkogenez riskini hem de kötü prognoz olasılığını ve malignite meydana geldiğinde tedaviye direnç olasılığını artırabilir.
Demir şelatör desferoksamin mesilat (DFO) tarafından indüklenen hücresel demir tükenmesinin HIF-la’yı ( 112 ) arttırdığı gösterilmiştir . Transkripsiyon faktörü HIF-la, güçlü bir malign anjiyogenez ve metastaz indükleyicisi olan vasküler endotelyal büyüme faktörünün (VEGF) ekspresyonuna aracılık eder. Bu nedenle, demir eksikliği hem de meme kanseri HIF-1α stabilizasyon VEGF formasyonu, anjiyogenez ve tümör ilerlemesi üzerinde önemli etkilere sahip olduğu rapor edilmiştir , in vitro ve in vivo çalışmalar ( 68 , 113 ). Jacobsen ve ark. ( 114) artan VEGF düzeylerinin insan renal hücreli karsinomda kötü bir sonuçla ilişkili olduğunu bulmuştur. Ayrıca, bu modellerden birinde, demir takviyesinin hipokside VEGF seviyelerini önemli ölçüde azalttığı bulundu, bu da demirin HIF-la stabilizasyonuna karşı koymada ve dolayısıyla muhtemelen anjiyojenezi önlemede bir rolü olduğunu gösterir ( 113 ).
Miyeloperoksidaz (MPO) ve NADPH oksidaz, monositler tarafından interferon-y (IFN-γ) indüksiyonunda ve nötrofillerde ROS üretimi yoluyla mikrobiyal öldürme ve fagositozda anahtar rol oynayan enzimlerdir. Bu enzimler demire bağımlıdır ( 115 – 118 ): Demir eksikliği olduğunda katalitik aktiviteleri baskılanarak fagositozun bozulmasına neden olur. Sonuç olarak, enfeksiyonlara duyarlılık ve tümör gelişimi artabilir ( 20 , 118 ).
Doğal öldürücü (NK) hücreler, doğuştan gelen bağışıklık sistemi içinde bağışıklık denetimi ve anti-tümör eylemleri dahil olmak üzere benzersiz işlevleri yerine getiren sitotoksik efektör lenfositlerdir ( 119 ). Demir eksikliği durumunun özelliği olan hipoksinin, hayati aktive edici NK-hücre reseptörlerinin ve NK-hücre ligandlarının tümör hücre zarları üzerindeki ekspresyonunu inhibe ettiği gösterilmiştir ( 120 , 121 ). Bu nedenle demir eksikliği, NK hücrelerinin sitotoksik ve spesifik olarak anti-tümör aktivitelerini bozar ve onkogenez ve tümör büyümesine yardımcı olur.
Doğal öldürücü hücreler, T hücreleri ve B hücrelerinden oluşan lenfositler, hücre aracılı bağışıklığın başlıca hücresel bileşenleridir. Sitotoksik T hücrelerinin, biri tümör hücrelerinin parçalanması olan çeşitli işlevleri vardır. Demir eksikliğinin, T hücresi proliferasyonunu ve güçlü anti-tümör sitokin IFN-y’nin salgılanmasını engellediği gösterilmiştir ( 122 ). Fare modellerinde, demir eksikliğinin timus bezinin atrofisine ve CD28 timositlerinin ve dalak hücrelerinin atılımının azalmasına yol açarak lenfositik hareketlilik ve işlevlerde bozulmaya neden olduğu bulundu ( 123 , 124 ). Ek olarak, demir eksikliği durumunda T hücre göçü ve immünolojik sinaps için hayati önem taşıyan sitozolden plazma zarına protein kinaz-C translokasyonu azalır ( 125)., 126 ). Ayrıca, demir eksikliği, bağışıklık sistemi hücrelerinden çeşitli farklı etki gösteren sitokinlerin ekspresyonunu genel olarak engeller ( 127 – 129 ). Bu nedenle hücre aracılı bağışıklık, demir eksikliği nedeniyle bozulur ve kanser gelişimi ve büyümesinin önünü açar.
Hücre içi demirin HCT-116 (insan kanseri) hücrelerinin apoptozunda anahtar bir rol oynadığı gösterilmiştir ( 130 ). Ayrıca, apoptoz direncinin önemli bir belirteci olan sitokrom-c oksidaz aktivitesi, demir eksikliği varlığında belirgin bir şekilde azalır ( 131 , 132 ). Bu nedenle, demir eksikliğinin kansere bağlı etkileri, sadece tümör gelişimini ve ilerlemesini değil, aynı zamanda apoptoz ve tedavi yanıtını da etkileyebilir.Git:
Kolorektal Kanser İlişkili Demir Eksikliği Anemisinin İnsan Klinik Çalışmalarından Elde Edilen Kanıtlar
Demir eksikliğinin kanserle ilgili önemli etkilerini açıklayan bol miktarda biyolojik ve immünolojik kanıtın insan sağlığı üzerinde doğrudan etkileri vardır. Klinik ve epidemiyolojik çalışmalar, demir eksikliği ile KRK arasındaki ilişkinin etiyolojiden progresyona ve metastaza, terapötik yanıta ve uzun vadeli sonuçlara kadar çeşitli yönlerine odaklanmıştır.
CRC’li hastalarla ilgili çalışmalar, Kaliforniyalı erkeklerden oluşan bir kohortta ( 133 ) düşük transferrin satürasyonu ile ve New York’lu kadınlarda vaka kontrollü iç içe bir çalışmada ( 134 ) düşük serum ferritin ile anlamlı bir ilişki bulmuştur . Başka bir kohort çalışmasında, normal hemoglobin (Hb) ve TSAT seviyelerine sahip bireylere kıyasla, demir eksikliği anemisi olmayan erkeklerde ve postmenopozal kadınlarda beş kat ve DEA’lılarda gastrointestinal kanser gelişme riski 31 kat artmıştır ( 15 ).
50-75 yaşları arasındaki 965 erkek ve kadından oluşan geniş bir kohortta Bird ve ark. ( 135 ), yüksek (>27.3 mg/gün) veya düşük (<11,6 mg/gün) demir tüketenlerin kolorektal polip geliştirme olasılığının daha yüksek olduğu, demir alımı ile kolorektal polipler arasında U şeklinde bir ilişki bulmuştur. CRC. Buna paralel olarak, Cross ve ark. ( 136 ), CRC riskinin serum ferritin seviyeleri ile ters orantılı ve serum doymamış demir bağlama kapasitesi (UIBC) ile pozitif ilişkili olduğunu gösterdi. Ayrıca serum demiri ve TSAT’ın özellikle kolon kanseri riski ile ters bir ilişkisi olduğu bulundu ( 136 ). Hamarneh ve ark. ( 137) pozitif bir fekal immünokimyasal testin ardından CRC için risk faktörlerini değerlendirirken, IDA, yaştan bağımsız olarak CRC için önemli bir risk faktörü olarak rapor edildi [OR 7.93, %95 Cl (2.90–21.69), p < 0.001]. Yukarıdaki bulgular, aşırı demir alımının yaptığı gibi, demir eksikliğinin CRC patogenezine katkıda bulunabileceğini öne sürse de, mekanizmalar henüz tam olarak anlaşılmamıştır. Bununla birlikte, yukarıda sunulduğu gibi, klinik öncesi araştırmalar, demir eksikliğinin bağışıklık tepkisini köreltme, azalan bağışıklık gözetimi altında tümör hücresi istilasına izin verme veya tümör mikroçevresinde bir pro-tümorijenik bağışıklık hücresi işlevine geçiş yapma rolüne işaret etmektedir ( 4 , 9 , 22 , 23 ) ).
Demir eksikliği sadece onkogenezi önemli ölçüde etkilemekle kalmaz, aynı zamanda CRC’li hastalarda onkolojik sonuçları da etkilediği bulunmuştur. Zhen et al. ( 138 ), TNM evre II CRC’li 644 hastanın (19-83 yıl) sonuçları üzerinde demir eksikliğinin uzun vadeli etkilerini araştırdı ve IDA’nın T3N0M0 evre kolon kanserli hastalarda uzun vadeli sonucun bağımsız bir öngörücüsü olduğunu buldu. DEA’lı hastalar daha kötü sonuçlara sahipti ve anemik olmayan hastalara göre daha kötü tümör evrelemesi ve daha düşük hastalıksız sağkalım ile sunuldu ( 138). Bu bulgular, IDA’nın, muhtemelen tümör büyümesini sınırlayan bağışıklık sistemi mekanizmalarını inhibe ederek, kemoterapi veya cerrahi gibi tedavilere yanıtı engelleyerek ve bağışıklık sisteminin, uzak metastaza dönüşebilen dolaşımdaki tümör hücrelerine yanıtını kısıtlayarak, CRC prognozunu ve sonuçlarını etkileyebileceğini düşündürmektedir. 4 , 9 , 139 ). Lorenzi ve ark. ( 140 ), küratif veya palyatif cerrahi uygulanan hem yüksek hem de düşük serum ferritin seviyelerine sahip hastaların, normal seviyelere kıyasla en az 5 yıllık bir takip süresinden sonra daha kısa sağkalıma sahip olduğunu bulmuşlardır. An ve ark. ( 141), kombine FOLFOX bazlı adjuvan kemoterapi ile tedavi edilen preoperatif anemisi olan hastaların anemisi olmayanlara göre daha kötü prognoza sahip olduğunu gösterdi. Ek olarak, 60 çalışmanın sistematik bir incelemesi, anemisi olan kanser hastaları arasında anemisi olmayanlara kıyasla genel olarak %65 yüksek mortalite riski tespit etti ( 19 ).
Bu nedenle, genel olarak, epidemiyolojik ve klinik araştırmalardan elde edilen kanıtlar, preklinik çalışmalardan elde edilen verileri doğrular ve demir eksikliği gibi demir eksikliğinin onkogenez, tümör ilerlemesi ve bireysel sonuçlar açısından önemli ölçüde olumsuz bir etkiye sahip olabileceğini düşündürür. Anemili veya anemisiz demir eksikliği, CRC’li hastalarda kötü prognoz, daha kötü tümör evrelemesi, daha düşük hastalıksız sağkalım oranları ve onkolojik tedavilere daha kötü yanıt ile ilişkilidir.Git:
Terapötik Bıçak Kenarında: Kolorektal Kanserli ve Demir Eksikliği/Anemisi Olan Hastalarda Demir Replasman Tedavisi
Şu anda CRC bağlamında demir eksikliği için üç ana tedavi yaklaşımı vardır; kan transfüzyonları (RBC transfüzyonları), eritropoezi uyarıcı ajanlar (ESA’lar) ve demir takviyesi ( 26 , 34 ). Hem RBC transfüzyonları hem de ESA’lar, demir eksikliği/anemi gibi, bağımsız olarak artan bir CRC nüksü ve mortalite riski ile ilişkili olduğundan ( 142 – 144 ), anemiyi tersine çevirmek için demir ikame tedavisinin kullanımı daha fazla dikkat çekmiştir. Prensip olarak, demir oral veya intravenöz olarak değiştirilebilir.
oral demir
Demirin oral ikamesi, basitliği ve düşük maliyetleri nedeniyle ve erken intravenöz demir bileşikleri ile ilişkili advers olaylar nedeniyle devam eden güvenlik endişelerinin bir sonucu olarak uzun süredir tercih edilmektedir. Bununla birlikte, kanser hastalarında uygunluğu genellikle eşzamanlı inflamasyon, gastrointestinal rahatsızlık ve çoklu ilaç kullanımı ile sınırlıdır. Ayrıca, oral demir kanserli hastalarda tutarlı klinik veya hematolojik iyileşme ile ilişkilendirilmemiştir ( 82 , 145 – 147 ). Tam aksine; Bu hastalarda bağırsak demir emilimi büyük ölçüde azaldığından (demirin yaklaşık %95’i atılır) ( 33 ) kanserli bireylerde ve özellikle CRC’li bireylerde etkisiz olduğu bulunmuştur.). Ayrıca, bağırsaktaki demir emiliminin azalması nedeniyle bağırsakta artan demir mevcudiyeti, hastalığın ilerlemesini engelleme olasılığı daha yüksek olan koruyucu yolcu bakterileri yerine tümörün ilerlemesine neden olan patojenik bağırsak bakterilerinin çoğalmasını destekleyebilir ( 148 ). Emilen çok az miktarda demire gelince, çoğu, inflamatuar sitokinler tarafından büyük ölçüde bloke edildiği ve dolayısıyla metabolize edilemediği enterositlerde hapsolmuş halde kalır ( 33 , 149 ). Bu nedenle, genel olarak oral demir, CRC’li hastalarda demir replasmanı için uygun değildir.
intravenöz demir
Demir doğrudan makrofajlar tarafından tutulduğu için intravenöz (IV) demir, demirin emici inflamatuar blokajını yenebilir ( 33 ). Kanser (hastalarında (ek ESA’lar olmadan) IV ile demir tedavisinin destek yararları giderek artan kanıtlar bulunmaktadır , 150 – 160 CRC (hastalarında spesifik olarak ameliyat öncesi hemoglobin seviyeleri optimize etmek için gösterilmiştir, IV demir) 158 – 163 ). Öte yandan, genişletilmiş IVICA çalışmasında, preoperatif olarak oral veya IV demir ile tedavi edilen anemi ve kolorektal kanserli 116 hastayı içeren randomize bir çalışmada, 5 yıllık genel sağkalım veya hastalıksız sağkalım için anlamlı bir fark bulunmadı ( 164). Tümör büyümesinin desteklenmesi, artan oksidatif stres ve zayıf hastalık ilerlemesi dahil olmak üzere kanserde aşırı demir yükünün olası rolü hakkında bazı endişeler vardır ( 165 – 167 ). Wilson ve ark. ( 168 ) “demir tedavisinin kolorektal tümör büyümesini destekleyerek ve metastatik potansiyeli artırarak kolorektal tümör prognozunu kötüleştirebileceğini” öne sürüyor. Bununla birlikte, bu hipotezi doğrulamak için deneysel çalışmalardan elde edilen doğrudan bir kanıt yoktur ve bu tür deneysel verilerin kanserli hastalarda klinik uygulanabilirliği sınırlıdır, çünkü bunlar yüksek demir dozlarına, farklı enjeksiyon yollarına ve çeşitli demir formülasyonlarına dayanmaktadır. tipik olarak klinik ortamlarda kullanılmaz ( 27 , 169). Ayrıca kanserli hastalarda aşırı demir yüklenmesi nadirdir ( 34 ).
Yüksek oral demir alım tümörlerin oluşumunu arttırdığı gösterilmiştir, oysa enflamatuar veya karsinojenik ajanların neden olduğu CRC kemirgen modellerinde, sistemik (IV) ‘ün demir desteği aynı etkiye (yoktu 170 , 171 ). Bu, artan lümen demirinin, sistemik demir düzeylerinin değil, CRC’nin inflamatuar modellerinde kolorektal karsinogenezi arttırdığını göstermektedir ( 172 , 173 ). Radulescu ve ark., bir kemirgen modelinde luminal demirin Apc ( adenomatöz polipozis koli geni) ile işbirliği yaptığını göstermiştir.) bağırsak tümör oluşumunu teşvik etmek için kayıp, CRC’li hastalarda kolonik luminal demir şelasyonu ve eşzamanlı sistemik demir replasman tedavisinin bir kombinasyonunun hem anemiyi çözeceğini hem de kolondaki kanserojen kalıntı demir havuzunu azaltacağını öne sürüyor ( 174 ).
Onkolojik bir popülasyonda IV demir tedavisinin (tek başına veya ESA’larla kombinasyon halinde) sonuçlarını açıklayan prospektif klinik çalışmalardan elde edilen kanıtlar nispeten azdır, ancak sonuçları kemirgen modeli çalışmalarının bulguları ile uyumludur. IV demir ve ESA’lar ile tedavi edilen hastalarda tümör progresyonunun arttığını göstermediği için kısa süreli çalışmalar güven vericidir ( 34 ). Kanserli hastalarda IV demir ve ESA tedavisini değerlendiren bir prospektif randomize kontrollü çalışma ( 175), 1,4 yıllık medyan takip süresi ile uzun vadeli sonuçlar veya sağkalım üzerinde herhangi bir olumsuz etki bulamadı. Uzatılmış bir takip süresi (medyan 3.9 yıl) ile CRC için cerrahi uygulanan hastaların retrospektif bir kohort çalışması, IV demir (bu durumda, ferrik karboksimaltoz) ile tedavi edilen deneklerde genel ve hastalıksız sağkalımın önemli ölçüde farklılık göstermediğini doğrulamıştır. IV demir almayan eşleşen bir grupla karşılaştırıldığında 1.000-2.000 mg’lık bir dozda ( 176 ). Gilreath ve ark. tarafından demir dekstran kullanımının kapsamlı bir incelemesi. aşırı demir yüklenmesi nedeniyle kanser büyümesi riskinin artmasını destekleyen hiçbir klinik kanıt olmadığı sonucuna varmıştır ( 167 ).
Enfeksiyon riski ile ilgili olarak, IV demir ile tedavi edilen kanserli hastalarda endişe verici bir belirti ortaya çıkmamıştır. Bununla birlikte, demirin bağışıklık tepkisi ve mikrobiyal çoğalmadaki rolü göz önüne alındığında ( 177 ), mevcut kılavuzlar ihtiyatlı bir şekilde aktif enfeksiyonları olan veya olduğundan şüphelenilen hastalara IV demir uygulanmamasını tavsiye etmektedir ( 34 ).
IV demir tedavisi ile bağlantılı olarak kardiyovasküler morbiditede herhangi bir artış gözlenmemiştir ( 82 , 145 , 178 – 180 ). Bununla birlikte, IV demir ve kardiyotoksik kemoterapinin birlikte uygulanmasından kaçınılması önerilir: IV demir, kemoterapi uygulamasından önce veya sonra veya kemoterapi tedavi döngüsünün sonunda uygulanmalıdır ( 34 ).Git:
Çözüm
Onkogenezin olası (birlikte) tetikleyicisi ve itici gücü olarak aşırı demirin etkilerine halihazırda ayrılmış olan büyük miktarda araştırmanın aksine, demir eksikliğinin rolü büyük ölçüde ihmal edilmiştir ve – gözden geçirilmiş klinik öncesi ve klinik verilerin kanıtlarına göre — muhtemelen hafife alınmıştır. Özellikle demir, bağışıklık sisteminin optimal işleyişi için hayati öneme sahiptir ve çok sayıda farklı bağışıklık süreci ve yolunda önemli roller oynar. Demir eksikliği, habis transformasyona ve tümör büyümesine karşı savunmanın anahtarı olan bağışıklık gözetimi, gen regülasyonu ve hücre apoptozisi gibi önemli mekanizmaları etkiler. Kanser ve demir eksikliği/anemisi olan hastalarda yapılan klinik çalışmalar, oral demirden farklı olarak, IV demir tedavisi (ESA’larla birlikte/olmadan), enfeksiyon veya kardiyovasküler morbidite riskini artırmadan genel sonuçları iyileştirir. Fazla (yutulmamış/artık) oral demir, bağırsak yolunda onkojenik etkilere neden olabilir ve bu nedenle genellikle CRC’li hastalar için uygun değildir (“savunmacı” dozlama stratejileri kullanılarak kullanımı zaman zaman haklı gösterilebilse de). Genel olarak, IV demir, kemirgen çalışmalarıyla onaylandığı gibi, bu yerel alevlenme potansiyeline sahip görünmüyor. Kanserli hastalarda aşırı demir yüklenmesi nadiren görülür ve IV demirin tümör progresyonunu olumsuz etkilediğine dair klinik bir kanıt yoktur. Bununla birlikte, aşırı demir yükünün tümör büyümesi üzerindeki etkilerine dair çok sayıda kanıt göz önüne alındığında, anemiden kaçınmak ve demir depolarını korumak amacıyla IV demirin dikkatli bir şekilde desteklenmesi gerektiğini öneriyoruz.Git:
Yazar Katkıları
AA ilk literatür araştırmasını yaptı. Tüm yazarlar veri analizine, makale taslağının hazırlanmasına katıldı, önemli entelektüel içerik için makaleyi gözden geçirdi ve teslim için nihai versiyonu onayladı.Git:
Çıkar çatışması
AA: Kongre giderleri, danışmanlık ve ders ücretleri: Vifor Pharma ve Immundiagnostik AG. KF: Konuşmacıların ücreti: Immundiagnostik AG. İşletim Sistemi: Kongre masrafları: Abbvie, Falk, Janssen, Takeda; Ders ücretleri: Abbvie, Falk, Janssen, Takeda, Norgine, Pfizer. JS: Danışmanlık: Pharmacosmos, Vifor. Abbvie, Bristol Myers Squibb, Dr Schär, Falk, Ferring, Fresenius Kabi, Immundiagnostik, Janssen, Medice, MSD, Pfizer, Shire, Takeda, Thermofisher. Yönetim Kurulu Üyesi: Pharmacosmos, Vifor, Abbvie, Bristol Myers Squibb, Dr Schär, Ferring, Fresenius Kabi, Immundiagnostik, Janssen, MSD, NPS, Takeda, Shield. Anlatım: Vifor. Kalan yazarlar, araştırmanın potansiyel bir çıkar çatışması olarak yorumlanabilecek herhangi bir ticari veya finansal ilişkinin yokluğunda yürütüldüğünü beyan eder.Git:
Teşekkür
Yazarlar, el yazmasının düzenlenmesi ve düzeltilmesinde Janet Collins’in (Interdisziplinäres Crohn Colitis Centrum Rhein-Main, Frankfurt am Main, Almanya) yardımına minnetle teşekkür eder.Git:
Sözlük
Kısaltmalar
| YARDIM | mutlak demir eksikliği |
| KEDİ | katalaz |
| CHr | retikülositlerin hemoglobin içeriği |
| CRC | kolorektal kanser |
| EMT | epitelden mezenkimal geçişe |
| ESA | eritropoezi uyarıcı madde |
| Fe-S kümesi | demir-kükürt kümesi |
| FID | fonksiyonel demir eksikliği |
| GSH-Px | Glutatyon peroksidazı |
| Hb | hemoglobin |
| HIF | hipoksi ile indüklenebilir faktör |
| IDA | demir eksikliği anemisi |
| EĞER | interferon |
| IL | interlökin |
| JHDM | Jumonji-C (JmjC)-alan içeren histon demetilaz |
| MCV | ortalama korpüsküler hacim |
| miRNA | mikroRNA |
| NF | nükleer faktör |
| NK | doğal katil |
| MPO | miyeloperoksidaz |
| RBC | kırmızı kan hücresi |
| REDOX | oksidasyon redüksiyon |
| bilimkurgu | serum ferritini |
| SOD | süperoksit dismutaz |
| TNF | tümör nekroz faktörü |
| TSAT | transferrin doygunluğu |
| ZnPP | çinko protoporfirin |
| sTfR | çözünür transferrin reseptörü |
| UIBC | doymamış demir bağlama kapasitesi |
| VEGF | vasküler endotelyal büyüme faktörü |
| VHL | von Hippel-Lindau |
| %HİPO | hipokromik eritrositlerin yüzdesi. |
Referanslar
1. Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. (2018) 68:394–424. 10.3322/caac.21492 [PubMed] [CrossRef] [Google Scholar]2. Keum N, Giovannucci E. Global burden of colorectal cancer: emerging trends, risk factors and prevention strategies. Nat Rev Gastroenterol Hepatol. (2019) 16:713–32. 10.1038/s41575-019-0189-8 [PubMed] [CrossRef] [Google Scholar]3. Dekker E, Tanis PJ, Vleugels JLA, Kasi PM, Wallace MB. Colorectal cancer. Lancet. (2019) 394:1467–80. 10.1016/S0140-6736(19)32319-0 [PubMed] [CrossRef] [Google Scholar]4. Phipps O, Brookes MJ, Al-Hassi HO. Iron deficiency, immunology, and colorectal cancer. Nutr Rev. (2020) 79:88–97. 10.1093/nutrit/nuaa040 [PubMed] [CrossRef] [Google Scholar]5. Fonseca-Nunes A, Jakszyn P, Agudo A. Iron and cancer risk–a systematic review and meta-analysis of the epidemiological evidence. Cancer Epidemiol Biomarkers Prev. (2014) 23:12–31. 10.1158/1055-9965.EPI-13-0733 [PubMed] [CrossRef] [Google Scholar]6. Nelson RL. Iron and colorectal cancer risk: human studies. Nutr Rev. (2001) 59:140–8. 10.1111/j.1753-4887.2001.tb07002.x [PubMed] [CrossRef] [Google Scholar]7. Stevens RG, Jones DY, Micozzi MS, Taylor PR. Body iron stores and the risk of cancer. N Engl J Med. (1988) 319:1047–52. 10.1056/NEJM198810203191603 [PubMed] [CrossRef] [Google Scholar]8. Knekt P, Reunanen A, Takkunen H, Aromaa A, Heliövaara M, Hakulinen T. Body iron stores and risk of cancer. Int J Cancer. (1994) 56:379–82. 10.1002/ijc.2910560315 [PubMed] [CrossRef] [Google Scholar]9. Pfeifhofer-Obermair C, Tymoszuk P, Petzer V, Weiss G, Nairz M. Iron in the tumor microenvironment-connecting the dots. Front Oncol. (2018) 8:549. 10.3389/fonc.2018.00549 [PMC free article] [PubMed] [CrossRef] [Google Scholar]10. Brown RAM, Richardson KL, Kabir TD, Trinder D, Ganss R, Leedman PJ. Altered iron metabolism and impact in cancer biology, metastasis, and immunology. Front Oncol. (2020) 10:476. 10.3389/fonc.2020.00476 [PMC free article] [PubMed] [CrossRef] [Google Scholar]11. Ganz T. Iron and infection. Int J Hematol. (2018) 107:7–15. 10.1007/s12185-017-2366-2 [PubMed] [CrossRef] [Google Scholar]12. Torti SV, Manz DH, Paul BT, Blanchette-Farra N, Torti FM. Iron and cancer. Annu Rev Nutr. (2018) 38:97–125. 10.1146/annurev-nutr-082117-051732 [PMC free article] [PubMed] [CrossRef] [Google Scholar]13. Jung M, Mertens C, Tomat E, Brüne B. Iron as a central player and promising target in cancer progression. Int J Mol Sci. (2019) 20:273. 10.3390/ijms20020273 [PMC free article] [PubMed] [CrossRef] [Google Scholar]14. Vela D. Iron in the tumor microenvironment. Adv Exp Med Biol. (2020) 1259:39–51. 10.1007/978-3-030-43093-1_3 [PubMed] [CrossRef] [Google Scholar]15. Ioannou GN, Rockey DC, Bryson CL, Weiss NS. Iron deficiency and gastrointestinal malignancy: a population-based cohort study. Am J Med. (2002) 113:276–80. 10.1016/S0002-9343(02)01214-7 [PubMed] [CrossRef] [Google Scholar]16. James MW, Chen CM, Goddard WP, Scott BB, Goddard AF. Risk factors for gastrointestinal malignancy in patients with iron-deficiency anaemia. Eur J Gastroenterol Hepatol. (2005) 17:1197–203. 10.1097/00042737-200511000-00008 [PubMed] [CrossRef] [Google Scholar]17. Ludwig H, Müldür E, Endler G, Hübl W. Prevalence of iron deficiency across different tumors and its association with poor performance status, disease status and anemia. Ann Oncol. (2013) 24:1886–92. 10.1093/annonc/mdt118 [PMC free article] [PubMed] [CrossRef] [Google Scholar]18. Paitan V, Alcarraz C, Leonardo A, Valencia G, Mantilla R, Morante Z, et al. . Anemia as a prognostic factor in cancer patients. Rev Peru Med Exp Salud Publica. (2018) 35:250–8. 10.17843/rpmesp.2018.352.3171 [PubMed] [CrossRef] [Google Scholar]19. Caro JJ, Salas M, Ward A, Goss G. Anemia as an independent prognostic factor for survival in patients with cancer: a systemic, quantitative review. Cancer. (2001) 91:2214–21. 10.1002/1097-0142(20010615)91:12<2214::AID-CNCR1251>3.0.CO;2-P [PubMed] [CrossRef] [Google Scholar]20. Zohora F, Bidad K, Pourpak Z, Moin M. Biological and immunological aspects of iron deficiency anemia in cancer development: a narrative review. Nutr Cancer. (2018) 70:546–56. 10.1080/01635581.2018.1460685 [PubMed] [CrossRef] [Google Scholar]21. Nakama H, Zhang B, Fattah AS, Zhang X. Colorectal cancer in iron deficiency anemia with a positive result on immunochemical fecal occult blood. Int J Colorectal Dis. (2000) 15:271–4. 10.1007/s003840000255 [PubMed] [CrossRef] [Google Scholar]22. Rieger MA, Schroeder T. Hematopoiesis. Cold Spring Harb Perspect Biol. (2012) 4:a008250. 10.1101/cshperspect.a008250 [PMC free article] [PubMed] [CrossRef] [Google Scholar]23. Muckenthaler MU, Rivella S, Hentze MW, Galy B. A red carpet for iron metabolism. Cell. (2017) 168:344–61. 10.1016/j.cell.2016.12.034 [PMC free article] [PubMed] [CrossRef] [Google Scholar]24. Ludwig H, Van Belle S, Barrett-Lee P, Birgegård G, Bokemeyer C, Gascón P, et al. . The European Cancer Anaemia Survey (ECAS): a large, multinational, prospective survey defining the prevalence, incidence, and treatment of anaemia in cancer patients. Eur J Cancer. (2004) 40:2293–306. 10.1016/j.ejca.2004.06.019 [PubMed] [CrossRef] [Google Scholar]25. Ploug M, Kroijer R, Qvist N, Lindahl CH, Knudsen T. Iron deficiency in colorectal cancer patients: a cohort study on prevalence and associations. Colorectal Dis. (2020). 10.1111/codi.15467. Epub ahead of print. [PubMed] [CrossRef] [Google Scholar]26. Abiri B, Vafa M. Iron deficiency and anemia in cancer patients: the role of iron treatment in anemic cancer patients. Nutr Cancer. (2020) 72:864–72. 10.1080/01635581.2019.1658794 [PubMed] [CrossRef] [Google Scholar]27. Busti F, Marchi G, Ugolini S, Castagna A, Girelli D. Anemia and iron deficiency in cancer patients: role of iron replacement therapy. Pharmaceuticals. (2018) 11:94. 10.3390/ph11040094 [PMC free article] [PubMed] [CrossRef] [Google Scholar]28. Ganz T, Nemeth E. Iron homeostasis in host defence and inflammation. Nat Rev Immunol. (2015) 15:500–10. 10.1038/nri3863 [PMC free article] [PubMed] [CrossRef] [Google Scholar]29. Grotto HZ. Anaemia of cancer: an overview of mechanisms involved in its pathogenesis. Med Oncol. (2008) 25:12–21. 10.1007/s12032-007-9000-8 [PubMed] [CrossRef] [Google Scholar]30. Ueda N, Takasawa K. Role of hepcidin-25 in chronic kidney disease: anemia and beyond. Curr Med Chem. (2017) 24:1417–52. 10.2174/0929867324666170316120538 [PubMed] [CrossRef] [Google Scholar]31. Ueda N, Takasawa K. Impact of inflammation on ferritin, hepcidin and the management of iron deficiency anemia in chronic kidney disease. Nutrients. (2018) 10:1173. 10.3390/nu10091173 [PMC free article] [PubMed] [CrossRef] [Google Scholar]32. Weiss G, Goodnough LT. Anemia of chronic disease. N Engl J Med. (2005) 352:1011–23. 10.1056/NEJMra041809 [PubMed] [CrossRef] [Google Scholar]33. Naoum FA. Iron deficiency in cancer patients. Rev Bras Hematol Hemoter. (2016) 38:325–30. 10.1016/j.bjhh.2016.05.009 [PMC free article] [PubMed] [CrossRef] [Google Scholar]34. Aapro M, Beguin Y, Bokemeyer C, Dicato M, Gascón P, Glaspy J, et al. . Management of anaemia and iron deficiency in patients with cancer: ESMO clinical practice guidelines. Ann Oncol. (2018) 29 (Suppl. 4):iv96–110. 10.1093/annonc/mdx758 [PubMed] [CrossRef] [Google Scholar]35. Grote Beverborg N, Klip IT, Meijers WC, Voors AA, Vegter EL, van der Wal HH, et al. . Definition of iron deficiency based on the gold standard of bone marrow iron staining in heart failure patients. Circ Heart Fail. (2018) 11:e004519. 10.1161/CIRCHEARTFAILURE.117.004519 [PubMed] [CrossRef] [Google Scholar]36. Hastka J, Lasserre JJ, Schwarzbeck A, Hehlmann R. Central role of zinc protoporphyrin in staging iron deficiency. Clin Chem. (1994) 40:768–73. 10.1093/clinchem/40.5.768 [PubMed] [CrossRef] [Google Scholar]37. Steinmetz HT, Tsamaloukas A, Schmitz S, Wiegand J, Rohrberg R, Eggert J, et al. . A new concept for the differential diagnosis and therapy of anaemia in cancer patients. Support Care Cancer. (2010) 19:261–9. 10.1007/s00520-010-0812-2 [PubMed] [CrossRef] [Google Scholar]38. Girelli D, Nemeth E, Swinkels DW. Hepcidin in the diagnosis of iron disorders. Blood. (2016) 127:2809–13. 10.1182/blood-2015-12-639112 [PMC free article] [PubMed] [CrossRef] [Google Scholar]39. Prentice AM, Doherty CP, Abrams SA, Cox SE, Atkinson SH, Verhoef H, et al. . Hepcidin is the major predictor of erythrocyte iron incorporation in anemic African children. Blood. (2012) 119:1922–8. 10.1182/blood-2011-11-391219 [PMC free article] [PubMed] [CrossRef] [Google Scholar]40. Munoz C, Rios E, Olivos J, Brunser O, Olivares M. Iron, copper and immunocompetence. Br J Nutr. (2007) 98 (Suppl. 1):S24–8. 10.1017/S0007114507833046 [PubMed] [CrossRef] [Google Scholar]41. Liu L, Huang M. Essential role of the iron-sulfur cluster binding domain of the primase regulatory subunit Pri2 in DNA replication initiation. Protein Cell. (2015) 6:194–210. 10.1007/s13238-015-0134-8 [PMC free article] [PubMed] [CrossRef] [Google Scholar]42. Dostal A, Lacroix C, Pham VT, Zimmermann MB, Del’homme C, Bernalier-Donadille A, et al. . Iron supplementation promotes gut microbiota metabolic activity but not colitis markers in human gut microbiota-associated rats. Br J Nutr. (2014) 111:2135–45. 10.1017/S000711451400021X [PubMed] [CrossRef] [Google Scholar]43. Bohnsack BL, Hirschi KK. Nutrient regulation of cell cycle progression. Annu Rev Nutr. (2004) 24:433–53. 10.1146/annurev.nutr.23.011702.073203 [PubMed] [CrossRef] [Google Scholar]44. Hentze MW, Muckenthaler MU, Galy B, Camaschella C. Two to tango: regulation of Mammalian iron metabolism. Cell. (2010) 142:24–38. 10.1016/j.cell.2010.06.028 [PubMed] [CrossRef] [Google Scholar]45. Dev S, Babitt JL. Overview of iron metabolism in health and disease. Hemodial Int. (2017) 21 (Suppl. 1):S6–s20. 10.1111/hdi.12542 [PMC free article] [PubMed] [CrossRef] [Google Scholar]46. Wang Y, Yu L, Ding J, Chen Y. Iron metabolism in cancer. Int J Mol Sci. (2018) 20:95. 10.3390/ijms20010095 [PMC free article] [PubMed] [CrossRef] [Google Scholar]47. Jung G, Hernández-Illán E, Moreira L, Balaguer F, Goel A. Epigenetics of colorectal cancer: biomarker and therapeutic potential. Nat Rev Gastroenterol Hepatol. (2020) 17:111–30. 10.1038/s41575-019-0230-y [PMC free article] [PubMed] [CrossRef] [Google Scholar]48. Sharma S, Kelly TK, Jones PA. Epigenetics in cancer. Carcinogenesis. (2010) 31:27–36. 10.1093/carcin/bgp220 [PMC free article] [PubMed] [CrossRef] [Google Scholar]49. Wainwright EN, Scaffidi P. Epigenetics and cancer stem cells: unleashing, hijacking, and restricting cellular plasticity. Trends Cancer. (2017) 3:372–86. 10.1016/j.trecan.2017.04.004 [PMC free article] [PubMed] [CrossRef] [Google Scholar]50. Camaschella C, Pagani A, Nai A, Silvestri L. The mutual control of iron and erythropoiesis. Int J Lab Hematol. (2016) 38 (Suppl. 1):20–6. 10.1111/ijlh.12505 [PubMed] [CrossRef] [Google Scholar]51. Wessels I. Epigenetics and metal deficiencies. Curr Nutr Rep. (2014) 3:196–203. 10.1007/s13668-014-0091-5 [CrossRef] [Google Scholar]52. Zhang C. Essential functions of iron-requiring proteins in DNA replication, repair and cell cycle control. Protein Cell. (2014) 5:750–60. 10.1007/s13238-014-0083-7 [PMC free article] [PubMed] [CrossRef] [Google Scholar]53. Prá D, Franke SI, Henriques JA, Fenech M. Iron and genome stability: an update. Mutat Res. (2012) 733:92–9. 10.1016/j.mrfmmm.2012.02.001 [PubMed] [CrossRef] [Google Scholar]54. Paul VD, Lill R. Biogenesis of cytosolic and nuclear iron-sulfur proteins and their role in genome stability. Biochim Biophys Acta. (2015) 1853:1528–39. 10.1016/j.bbamcr.2014.12.018 [PubMed] [CrossRef] [Google Scholar]55. Park SY, Park J-W, Chun Y-S. Jumonji histone demethylases as emerging therapeutic targets. Pharmacol Res. (2016) 105:146–51. 10.1016/j.phrs.2016.01.026 [PubMed] [CrossRef] [Google Scholar]56. Tausendschön M, Dehne N, Brüne B. Hypoxia causes epigenetic gene regulation in macrophages by attenuating Jumonji histone demethylase activity. Cytokine. (2011) 53:256–62. 10.1016/j.cyto.2010.11.002 [PubMed] [CrossRef] [Google Scholar]57. McCann TS, Sobral LM, Self C, Hsieh J, Sechler M, Jedlicka P. Biology and targeting of the Jumonji-domain histone demethylase family in childhood neoplasia: a preclinical overview. Expert Opin Ther Targets. (2019) 23:267–80. 10.1080/14728222.2019.1580692 [PMC free article] [PubMed] [CrossRef] [Google Scholar]58. Zamani M, Hosseini SV, Mokarram P. Epigenetic biomarkers in colorectal cancer: premises and prospects. Biomarkers. (2018) 23:105–14. 10.1080/1354750X.2016.1252961 [PubMed] [CrossRef] [Google Scholar]59. Liu Z, Wu R, Li G, Sun P, Xu Q, Liu Z. MiR-592 inhibited cell proliferation of human colorectal cancer cells by suppressing of CCND3 expression. Int J Clin Exp Med. (2015) 8:3490–7. [PMC free article] [PubMed] [Google Scholar]60. Okugawa Y, Grady WM, Goel A. Epigenetic alterations in colorectal cancer: emerging biomarkers. Gastroenterology. (2015) 149:1204–25.e12. 10.1053/j.gastro.2015.07.011 [PMC free article] [PubMed] [CrossRef] [Google Scholar]61. Calin GA, Sevignani C, Dumitru CD, Hyslop T, Noch E, Yendamuri S, et al. . Human microRNA genes are frequently located at fragile sites and genomic regions involved in cancers. Proc Natl Acad Sci USA. (2004) 101:2999–3004. 10.1073/pnas.0307323101 [PMC free article] [PubMed] [CrossRef] [Google Scholar]62. Weitz SH, Gong M, Barr I, Weiss S, Guo F. Processing of microRNA primary transcripts requires heme in mammalian cells. Proc Natl Acad Sci USA. (2014) 111:1861–6. 10.1073/pnas.1309915111 [PMC free article] [PubMed] [CrossRef] [Google Scholar]63. Bandara KV, Michael MZ, Gleadle JM. MicroRNA biogenesis in hypoxia. Microrna. (2017) 6:80–96. 10.2174/2211536606666170313114821 [PubMed] [CrossRef] [Google Scholar]64. Nallamshetty S, Chan SY, Loscalzo J. Hypoxia: a master regulator of microRNA biogenesis and activity. Free Radic Biol Med. (2013) 64:20–30. 10.1016/j.freeradbiomed.2013.05.022 [PMC free article] [PubMed] [CrossRef] [Google Scholar]65. Bao B, Azmi AS, Li Y, Ahmad A, Ali S, Banerjee S, et al. . Targeting CSCs in tumor microenvironment: the potential role of ROS-associated miRNAs in tumor aggressiveness. Curr Stem Cell Res Ther. (2014) 9:22–35. 10.2174/1574888X113089990053 [PMC free article] [PubMed] [CrossRef] [Google Scholar]66. Bao B, Ahmad A, Li Y, Azmi AS, Ali S, Banerjee S, et al. . Targeting CSCs within the tumor microenvironment for cancer therapy: a potential role of mesenchymal stem cells. Expert Opin Ther Targets. (2012) 16:1041–54. 10.1517/14728222.2012.714774 [PubMed] [CrossRef] [Google Scholar]67. Schetter AJ, Leung SY, Sohn JJ, Zanetti KA, Bowman ED, Yanaihara N, et al. . MicroRNA expression profiles associated with prognosis and therapeutic outcome in colon adenocarcinoma. JAMA. (2008) 299:425–36. 10.1001/jama.299.4.425 [PMC free article] [PubMed] [CrossRef] [Google Scholar]68. Jian J, Yang Q, Dai J, Eckard J, Axelrod D, Smith J, et al. . Effects of iron deficiency and iron overload on angiogenesis and oxidative stress-a potential dual role for iron in breast cancer. Free Radic Biol Med. (2011) 50:841–7. 10.1016/j.freeradbiomed.2010.12.028 [PMC free article] [PubMed] [CrossRef] [Google Scholar]69. Jian J, Yang Q, Shao Y, Axelrod D, Smith J, Singh B, et al. . A link between premenopausal iron deficiency and breast cancer malignancy. BMC Cancer. (2013) 13:307. 10.1186/1471-2407-13-307 [PMC free article] [PubMed] [CrossRef] [Google Scholar]70. Wang Y, Shi J, Chai K, Ying X, Zhou BP. The role of snail in EMT and tumorigenesis. Curr Cancer Drug Targets. (2013) 13:963–72. 10.2174/15680096113136660102 [PMC free article] [PubMed] [CrossRef] [Google Scholar]71. Zhang X, Zhang W, Ma SF, Miasniakova G, Sergueeva A, Ammosova T, et al. . Iron deficiency modifies gene expression variation induced by augmented hypoxia sensing. Blood Cells Mol Dis. (2014) 52:35–45. 10.1016/j.bcmd.2013.07.016 [PMC free article] [PubMed] [CrossRef] [Google Scholar]72. Akça H, Polat A, Koca C. Determination of total oxidative stress and total antioxidant capacity before and after the treatment of iron-deficiency anemia. J Clin Lab Anal. (2013) 27:227–30. 10.1002/jcla.21589 [PMC free article] [PubMed] [CrossRef] [Google Scholar]73. Koskenkorva-Frank TS, Weiss G, Koppenol WH, Burckhardt S. The complex interplay of iron metabolism, reactive oxygen species, and reactive nitrogen species: insights into the potential of various iron therapies to induce oxidative and nitrosative stress. Free Radic Biol Med. (2013) 65:1174–94. 10.1016/j.freeradbiomed.2013.09.001 [PubMed] [CrossRef] [Google Scholar]74. Sies H. Oxidative stress: a concept in redox biology and medicine. Redox Biol. (2015) 4:180–3. 10.1016/j.redox.2015.01.002 [PMC free article] [PubMed] [CrossRef] [Google Scholar]75. Toblli JE, Cao G, Oliveri L, Angerosa M. Effects of iron deficiency anemia and its treatment with iron polymaltose complex in pregnant rats, their fetuses and placentas: oxidative stress markers and pregnancy outcome. Placenta. (2012) 33:81–7. 10.1016/j.placenta.2011.11.017 [PubMed] [CrossRef] [Google Scholar]76. Klaunig JE. Oxidative Stress and Cancer. Curr Pharm Des. (2018) 24:4771–8. 10.2174/1381612825666190215121712 [PubMed] [CrossRef] [Google Scholar]77. Datta S, Cano M, Ebrahimi K, Wang L, Handa JT. The impact of oxidative stress and inflammation on RPE degeneration in non-neovascular AMD. Prog Retin Eye Res. (2017) 60:201–18. 10.1016/j.preteyeres.2017.03.002 [PMC free article] [PubMed] [CrossRef] [Google Scholar]78. Chen X, Song M, Zhang B, Zhang Y. Reactive oxygen species regulate T cell immune response in the tumor microenvironment. Oxid Med Cell Longev. (2016) 2016:1580967. 10.1155/2016/1580967 [PMC free article] [PubMed] [CrossRef] [Google Scholar]79. Gill JG, Piskounova E, Morrison SJ. Cancer, oxidative stress, and metastasis. Cold Spring Harb Symp Quant Biol. (2016) 81:163–75. 10.1101/sqb.2016.81.030791 [PubMed] [CrossRef] [Google Scholar]80. Reuter S, Gupta SC, Chaturvedi MM, Aggarwal BB. Oxidative stress, inflammation, and cancer: how are they linked? Free Radic Biol Med. (2010) 49:1603–16. 10.1016/j.freeradbiomed.2010.09.006 [PMC free article] [PubMed] [CrossRef] [Google Scholar]81. Walter PB, Knutson MD, Paler-Martinez A, Lee S, Xu Y, Viteri FE, et al. . Iron deficiency and iron excess damage mitochondria and mitochondrial DNA in rats. Proc Natl Acad Sci USA. (2002) 99:2264–9. 10.1073/pnas.261708798 [PMC free article] [PubMed] [CrossRef] [Google Scholar]82. Auerbach M, Ballard H, Trout JR, McIlwain M, Ackerman A, Bahrain H, et al. . Intravenous iron optimizes the response to recombinant human erythropoietin in cancer patients with chemotherapy-related anemia: a multicenter, open-label, randomized trial. J Clin Oncol. (2004) 22:1301–7. 10.1200/JCO.2004.08.119 [PubMed] [CrossRef] [Google Scholar]83. Lill R, Dutkiewicz R, Freibert SA, Heidenreich T, Mascarenhas J, Netz DJ, et al. . The role of mitochondria and the CIA machinery in the maturation of cytosolic and nuclear iron-sulfur proteins. Eur J Cell Biol. (2015) 94:280–91. 10.1016/j.ejcb.2015.05.002 [PubMed] [CrossRef] [Google Scholar]84. Kaniak-Golik A, Skoneczna A. Mitochondria-nucleus network for genome stability. Free Radic Biol Med. (2015) 82:73–104. 10.1016/j.freeradbiomed.2015.01.013 [PubMed] [CrossRef] [Google Scholar]85. Thévenod F. Iron and its role in cancer defense: a double-edged sword. Met Ions Life Sci. (2018) 18:437–67. 10.1515/9783110470734-021 [PubMed] [CrossRef] [Google Scholar]86. Gozzelino R, Jeney V, Soares MP. Mechanisms of cell protection by heme oxygenase-1. Annu Rev Pharmacol Toxicol. (2010) 50:323–54. 10.1146/annurev.pharmtox.010909.105600 [PubMed] [CrossRef] [Google Scholar]87. Lai C, Loo G. Cellular iron depletion weakens induction of heme oxygenase-1 by cadmium. Int J Biochem Cell Biol. (2011) 43:88–97. 10.1016/j.biocel.2010.09.025 [PubMed] [CrossRef] [Google Scholar]88. Correia MA, Sinclair PR, De Matteis F. Cytochrome P450 regulation: the interplay between its heme and apoprotein moieties in synthesis, assembly, repair, and disposal. Drug Metab Rev. (2011) 43:1–26. 10.3109/03602532.2010.515222 [PMC free article] [PubMed] [CrossRef] [Google Scholar]89. Lin HL, Zhang H, Walker VJ, D’Agostino J, Hollenberg PF. Heme modification contributes to the mechanism-based inactivation of human cytochrome P450 2J2 by two terminal acetylenic compounds. Drug Metab Dispos. (2017) 45:990–9. 10.1124/dmd.117.075846 [PMC free article] [PubMed] [CrossRef] [Google Scholar]90. Zhu Y, Silverman RB. Revisiting heme mechanisms. A perspective on the mechanisms of nitric oxide synthase (NOS), Heme oxygenase (HO), and cytochrome P450s (CYP450s). Biochemistry. (2008) 47:2231–43. 10.1021/bi7023817 [PubMed] [CrossRef] [Google Scholar]91. Dhur A, Galan P, Hercberg S. Effects of different degrees of iron deficiency on cytochrome P450 complex and pentose phosphate pathway dehydrogenases in the rat. J Nutr. (1989) 119:40–7. 10.1093/jn/119.1.40 [PubMed] [CrossRef] [Google Scholar]92. Rao NJ, Jagadeesan V. Effect of long term iron deficiency on the activities of hepatic and extra-hepatic drug metabolising enzymes in Fischer rats. Comp Biochem Physiol B Biochem Mol Biol. (1995) 110:167–73. 10.1016/0305-0491(94)00109-8 [PubMed] [CrossRef] [Google Scholar]93. Yang C, Li C, Li M, Tong X, Hu X, Yang X, et al. . CYP2S1 depletion enhances colorectal cell proliferation is associated with PGE2-mediated activation of β-catenin signaling. Exp Cell Res. (2015) 331:377–86. 10.1016/j.yexcr.2014.12.008 [PubMed] [CrossRef] [Google Scholar]94. Atamna H, Killilea DW, Killilea AN, Ames BN. Heme deficiency may be a factor in the mitochondrial and neuronal decay of aging. Proc Natl Acad Sci USA. (2002) 99:14807–12. 10.1073/pnas.192585799 [PMC free article] [PubMed] [CrossRef] [Google Scholar]95. Wallace DC. A mitochondrial paradigm of metabolic and degenerative diseases, aging, and cancer: a dawn for evolutionary medicine. Annu Rev Genet. (2005) 39:359–407. 10.1146/annurev.genet.39.110304.095751 [PMC free article] [PubMed] [CrossRef] [Google Scholar]96. Inoue H, Hanawa N, Katsumata SI, Katsumata-Tsuboi R, Takahashi N, Uehara M. Iron deficiency induces autophagy and activates Nrf2 signal through modulating p62/SQSTM. Biomed Res. (2017) 38:343–50. 10.2220/biomedres.38.343 [PubMed] [CrossRef] [Google Scholar]97. Merikallio H, Pääkkö P, Kinnula VL, Harju T, Soini Y. Nuclear factor erythroid-derived 2-like 2 (Nrf2) and DJ1 are prognostic factors in lung cancer. Hum Pathol. (2012) 43:577–84. 10.1016/j.humpath.2011.05.024 [PubMed] [CrossRef] [Google Scholar]98. Solis LM, Behrens C, Dong W, Suraokar M, Ozburn NC, Moran CA, et al. . Nrf2 and Keap1 abnormalities in non-small cell lung carcinoma and association with clinicopathologic features. Clin Cancer Res. (2010) 16:3743–53. 10.1158/1078-0432.CCR-09-3352 [PMC free article] [PubMed] [CrossRef] [Google Scholar]99. Lau A, Villeneuve NF, Sun Z, Wong PK, Zhang DD. Dual roles of Nrf2 in cancer. Pharmacol Res. (2008) 58:262–70. 10.1016/j.phrs.2008.09.003 [PMC free article] [PubMed] [CrossRef] [Google Scholar]100. Menegon S, Columbano A, Giordano S. The dual roles of NRF2 in cancer. Trends Mol Med. (2016) 22:578–93. 10.1016/j.molmed.2016.05.002 [PubMed] [CrossRef] [Google Scholar]101. Leinonen HM, Kansanen E, Pölönen P, Heinäniemi M, Levonen AL. Role of the Keap1-Nrf2 pathway in cancer. Adv Cancer Res. (2014) 122:281–320. 10.1016/B978-0-12-420117-0.00008-6 [PubMed] [CrossRef] [Google Scholar]102. Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell. (2011) 144:646–74. 10.1016/j.cell.2011.02.013 [PubMed] [CrossRef] [Google Scholar]103. D’Ignazio L, Bandarra D, Rocha S. NF-κB and HIF crosstalk in immune responses. FEBS J. (2016) 283:413–24. 10.1111/febs.13578 [PMC free article] [PubMed] [CrossRef] [Google Scholar]104. Meteoglu I, Erdogdu IH, Meydan N, Erkus M, Barutca S. NF-KappaB expression correlates with apoptosis and angiogenesis in clear cell renal cell carcinoma tissues. J Exp Clin Cancer Res. (2008) 27:53. 10.1186/1756-9966-27-53 [PMC free article] [PubMed] [CrossRef] [Google Scholar]105. Wang L, Cherayil BJ. Ironing out the wrinkles in host defense: interactions between iron homeostasis and innate immunity. J Innate Immun. (2009) 1:455–64. 10.1159/000210016 [PMC free article] [PubMed] [CrossRef] [Google Scholar]106. Schito L, Semenza GL. Hypoxia-inducible factors: master regulators of cancer progression. Trends Cancer. (2016) 2:758–70. 10.1016/j.trecan.2016.10.016 [PubMed] [CrossRef] [Google Scholar]107. Deeb G, Vaughan MM, McInnis I, Ford LA, Sait SN, Starostik P, et al. . Hypoxia-inducible factor-1α protein expression is associated with poor survival in normal karyotype adult acute myeloid leukemia. Leuk Res. (2011) 35:579–84. 10.1016/j.leukres.2010.10.020 [PubMed] [CrossRef] [Google Scholar]108. Harrison LB, Chadha M, Hill RJ, Hu K, Shasha D. Impact of tumor hypoxia and anemia on radiation therapy outcomes. Oncologist. (2002) 7:492–508. 10.1634/theoncologist.7-6-492 [PubMed] [CrossRef] [Google Scholar]109. Vaupel P, Harrison L. Tumor hypoxia: causative factors, compensatory mechanisms, and cellular response. Oncologist. (2004) 9 (Suppl. 5):4–9. 10.1634/theoncologist.9-90005-4 [PubMed] [CrossRef] [Google Scholar]110. Ryan HE, Poloni M, McNulty W, Elson D, Gassmann M, Arbeit JM, et al. . Hypoxia-inducible factor-1alpha is a positive factor in solid tumor growth. Cancer Res. (2000) 60:4010–5. [PubMed] [Google Scholar]111. Elson DA, Ryan HE, Snow JW, Johnson R, Arbeit JM. Coordinate up-regulation of hypoxia inducible factor (HIF)-1alpha and HIF-1 target genes during multi-stage epidermal carcinogenesis and wound healing. Cancer Res. (2000) 60:6189–95. [PubMed] [Google Scholar]112. Dongiovanni P, Valenti L, Ludovica Fracanzani A, Gatti S, Cairo G, Fargion S. Iron depletion by deferoxamine up-regulates glucose uptake and insulin signaling in hepatoma cells and in rat liver. Am J Pathol. (2008) 172:738–47. 10.2353/ajpath.2008.070097 [PMC free article] [PubMed] [CrossRef] [Google Scholar]113. Eckard J, Dai J, Wu J, Jian J, Yang Q, Chen H, et al. . Effects of cellular iron deficiency on the formation of vascular endothelial growth factor and angiogenesis. Cancer Cell Int. (2010) 10:28. 10.1186/1475-2867-10-28 [PMC free article] [PubMed] [CrossRef] [Google Scholar]114. Jacobsen J, Grankvist K, Rasmuson T, Bergh A, Landberg G, Ljungberg B. Expression of vascular endothelial growth factor protein in human renal cell carcinoma. BJU Int. (2004) 93:297–302. 10.1111/j.1464-410X.2004.04605.x [PubMed] [CrossRef] [Google Scholar]115. Paino IM, Miranda JC, Marzocchi-Machado CM, Cesarino EJ, de Castro FA, de Souza AM. Phagocytosis, oxidative burst, and produced reactive species are affected by iron deficiency anemia and anemia of chronic diseases in elderly. Biol Trace Elem Res. (2009) 129:116–25. 10.1007/s12011-008-8303-8 [PubMed] [CrossRef] [Google Scholar]116. Winterbourn CC, Kettle AJ, Hampton MB. Reactive oxygen species and neutrophil function. Annu Rev Biochem. (2016) 85:765–92. 10.1146/annurev-biochem-060815-014442 [PubMed] [CrossRef] [Google Scholar]117. Yamaguchi R, Kawata J, Yamamoto T, Ishimaru Y, Sakamoto A, Ono T, et al. . Mechanism of interferon-gamma production by monocytes stimulated with myeloperoxidase and neutrophil extracellular traps. Blood Cells Mol Dis. (2015) 55:127–33. 10.1016/j.bcmd.2015.05.012 [PubMed] [CrossRef] [Google Scholar]118. Bergman M, Salman H, Pinchasi R, Straussberg R, Djaldetti M, Bessler H. Phagocytic capacity and apoptosis of peripheral blood cells from patients with iron deficiency anemia. Biomed Pharmacother. (2005) 59:307–11. 10.1016/j.biopha.2004.11.009 [PubMed] [CrossRef] [Google Scholar]119. Moretta L, Montaldo E, Vacca P, Del Zotto G, Moretta F, Merli P, et al. . Human natural killer cells: origin, receptors, function, and clinical applications. Int Arch Allergy Immunol. (2014) 164:253–64. 10.1159/000365632 [PubMed] [CrossRef] [Google Scholar]120. Balsamo M, Manzini C, Pietra G, Raggi F, Blengio F, Mingari MC, et al. . Hypoxia downregulates the expression of activating receptors involved in NK-cell-mediated target cell killing without affecting ADCC. Eur J Immunol. (2013) 43:2756–64. 10.1002/eji.201343448 [PubMed] [CrossRef] [Google Scholar]121. Schilling D, Tetzlaff F, Konrad S, Li W, Multhoff G. A hypoxia-induced decrease of either MICA/B or Hsp70 on the membrane of tumor cells mediates immune escape from NK cells. Cell Stress Chaperones. (2015) 20:139–47. 10.1007/s12192-014-0532-5 [PMC free article] [PubMed] [CrossRef] [Google Scholar]122. Bowlus CL. The role of iron in T cell development and autoimmunity. Autoimmun Rev. (2003) 2:73–8. 10.1016/S1568-9972(02)00143-X [PubMed] [CrossRef] [Google Scholar]123. Kuvibidila SR, Porretta C, Surendra Baliga B, Leiva LE. Reduced thymocyte proliferation but not increased apoptosis as a possible cause of thymus atrophy in iron-deficient mice. Br J Nutr. (2001) 86:157–62. 10.1079/BJN2001366 [PubMed] [CrossRef] [Google Scholar]124. Kuvibidila SR, Porretta C. Iron deficiency and in vitro iron chelation reduce the expression of cluster of differentiation molecule (CD)28 but not CD3 receptors on murine thymocytes and spleen cells. Br J Nutr. (2003) 90:179–89. 10.1079/BJN2003864 [PubMed] [CrossRef] [Google Scholar]125. Kuvibidila SR, Kitchens D, Baliga BS. In vivo and in vitro iron deficiency reduces protein kinase C activity and translocation in murine splenic and purified T cells. J Cell Biochem. (1999) 74:468–78. 10.1002/(SICI)1097-4644(19990901)74:3<468::AID-JCB14>3.0.CO;2-G [PubMed] [CrossRef] [Google Scholar]126. Klecha AJ, Salgueiro J, Wald M, Boccio J, Zubillaga M, Leonardi NM, et al. . In vivo iron and zinc deficiency diminished T- and B-selective mitogen stimulation of murine lymphoid cells through protein kinase C-mediated mechanism. Biol Trace Elem Res. (2005) 104:173–83. 10.1385/BTER:104:2:173 [PubMed] [CrossRef] [Google Scholar]127. Kuvibidila S, Warrier RP. Differential effects of iron deficiency and underfeeding on serum levels of interleukin-10, interleukin-12p40, and interferon-gamma in mice. Cytokine. (2004) 26:73–81. 10.1016/j.cyto.2003.12.010 [PubMed] [CrossRef] [Google Scholar]128. Kuvibidila S, Yu L, Ode D, Velez M, Gardner R, Warrier RP. Effects of iron deficiency on the secretion of interleukin-10 by mitogen-activated and non-activated murine spleen cells. J Cell Biochem. (2003) 90:278–86. 10.1002/jcb.10627 [PubMed] [CrossRef] [Google Scholar]129. Kuvibidila SR, Velez M, Gardner R, Penugonda K, Chandra LC, Yu L. Iron deficiency reduces serum and in vitro secretion of interleukin-4 in mice independent of altered spleen cell proliferation. Nutr Res. (2012) 32:107–15. 10.1016/j.nutres.2011.12.005 [PubMed] [CrossRef] [Google Scholar]130. Longpre J, Loo G. Inhibition of deoxycholate-induced apoptosis in iron-depleted HCT-116 cells. Apoptosis. (2012) 17:70–8. 10.1007/s10495-011-0655-4 [PubMed] [CrossRef] [Google Scholar]131. de Deungria M, Rao R, Wobken JD, Luciana M, Nelson CA, Georgieff MK. Perinatal iron deficiency decreases cytochrome c oxidase (CytOx) activity in selected regions of neonatal rat brain. Pediatr Res. (2000) 48:169–76. 10.1203/00006450-200008000-00009 [PubMed] [CrossRef] [Google Scholar]132. Payne CM, Holubec H, Bernstein C, Bernstein H, Dvorak K, Green SB, et al. . Crypt-restricted loss and decreased protein expression of cytochrome C oxidase subunit I as potential hypothesis-driven biomarkers of colon cancer risk. Cancer Epidemiol Biomarkers Prev. (2005) 14:2066–75. 10.1158/1055-9965.EPI-05-0180 [PubMed] [CrossRef] [Google Scholar]133. Herrinton LJ, Friedman GD, Baer D, Selby JV. Transferrin saturation and risk of cancer. Am J Epidemiol. (1995) 142:692–8. 10.1093/oxfordjournals.aje.a117698 [PubMed] [CrossRef] [Google Scholar]134. Kato I, Dnistrian AM, Schwartz M, Toniolo P, Koenig K, Shore RE, et al. . Iron intake, body iron stores and colorectal cancer risk in women: a nested case-control study. Int J Cancer. (1999) 80:693–8. 10.1002/(SICI)1097-0215(19990301)80:5<693::AID-IJC11>3.0.CO;2-G [PubMed] [CrossRef] [Google Scholar]135. Bird CL, Witte JS, Swendseid ME, Shikany JM, Hunt IF, Frankl HD, et al. . Plasma ferritin, iron intake, and the risk of colorectal polyps. Am J Epidemiol. (1996) 144:34–41. 10.1093/oxfordjournals.aje.a008852 [PubMed] [CrossRef] [Google Scholar]136. Cross AJ, Gunter MJ, Wood RJ, Pietinen P, Taylor PR, Virtamo J, et al. . Iron and colorectal cancer risk in the alpha-tocopherol, beta-carotene cancer prevention study. Int J Cancer. (2006) 118:3147–52. 10.1002/ijc.21780 [PubMed] [CrossRef] [Google Scholar]137. Hamarneh Z, Symonds EL, Kholmurodova F, Cock C. Older age, symptoms, or anemia: Which factors increase colorectal cancer risk with a positive fecal immunochemical test? J Gastroenterol Hepatol. (2020) 35:1002–8. 10.1111/jgh.14888 [PubMed] [CrossRef] [Google Scholar]138. Zhen L, Zhe S, Zhenning W, Zhifeng M, Zhidong L, Xiaoxia L, et al. . Iron-deficiency anemia: a predictor of diminished disease-free survival of T3N0M0 stage colon cancer. J Surg Oncol. (2012) 105:371–5. 10.1002/jso.22032 [PubMed] [CrossRef] [Google Scholar]139. Prá D, Rech Franke SI, Pegas Henriques JA, Fenech M. A possible link between iron deficiency and gastrointestinal carcinogenesis. Nutr Cancer. (2009) 61:415–26. 10.1080/01635580902803701 [PubMed] [CrossRef] [Google Scholar]140. Lorenzi M, Lorenzi B, Vernillo R. Serum ferritin in colorectal cancer patients and its prognostic evaluation. Int J Biol Markers. (2006) 21:235–41. 10.1177/172460080602100407 [PubMed] [CrossRef] [Google Scholar]141. An MS, Yoo JH, Kim KH, Bae KB, Choi CS, Hwang JW, et al. . T4 stage and preoperative anemia as prognostic factors for the patients with colon cancer treated with adjuvant FOLFOX chemotherapy. World J Surg Oncol. (2015) 13:64. 10.1186/s12957-015-0488-7 [PMC free article] [PubMed] [CrossRef] [Google Scholar]142. Acheson AG, Brookes MJ, Spahn DR. Effects of allogeneic red blood cell transfusions on clinical outcomes in patients undergoing colorectal cancer surgery: a systematic review and meta-analysis. Ann Surg. (2012) 256:235–44. 10.1097/SLA.0b013e31825b35d5 [PubMed] [CrossRef] [Google Scholar]143. Amato A, Pescatori M. Perioperative blood transfusions for the recurrence of colorectal cancer. Cochrane Database Syst Rev. (2006) 2006:CD005033. 10.1002/14651858.CD005033.pub2 [PMC free article] [PubMed] [CrossRef] [Google Scholar]144. Pascual M, Bohle B, Alonso S, Mayol X, Salvans S, Grande L, et al. . Preoperative administration of erythropoietin stimulates tumor recurrence after surgical excision of colon cancer in mice by a vascular endothelial growth factor-independent mechanism. J Surg Res. (2013) 183:270–7. 10.1016/j.jss.2012.12.041 [PubMed] [CrossRef] [Google Scholar]145. Henry DH, Dahl NV, Auerbach M, Tchekmedyian S, Laufman LR. Intravenous ferric gluconate significantly improves response to epoetin alfa versus oral iron or no iron in anemic patients with cancer receiving chemotherapy. Oncologist. (2007) 12:231–42. 10.1634/theoncologist.12-2-231 [PubMed] [CrossRef] [Google Scholar]146. Petrelli F, Borgonovo K, Cabiddu M, Lonati V, Barni S. Addition of iron to erythropoiesis-stimulating agents in cancer patients: a meta-analysis of randomized trials. J Cancer Res Clin Oncol. (2012) 138:179–87. 10.1007/s00432-011-1072-3 [PubMed] [CrossRef] [Google Scholar]147. Gafter-Gvili A, Rozen-Zvi B, Vidal L, Leibovici L, Vansteenkiste J, Gafter U, et al. . Intravenous iron supplementation for the treatment of chemotherapy-induced anaemia – systematic review and meta-analysis of randomised controlled trials. Acta Oncol. (2013) 52:18–29. 10.3109/0284186X.2012.702921 [PubMed] [CrossRef] [Google Scholar]148. Phipps O, Al-Hassi HO, Quraishi MN, Kumar A, Brookes MJ. Influence of iron on the gut microbiota in colorectal cancer. Nutrients. (2020) 12:2512. 10.3390/nu12092512 [PMC free article] [PubMed] [CrossRef] [Google Scholar]149. Ludwig H, Evstatiev R, Kornek G, Aapro M, Bauernhofer T, Buxhofer-Ausch V, et al. . Iron metabolism and iron supplementation in cancer patients. Wien Klin Wochenschr. (2015) 127:907–19. 10.1007/s00508-015-0842-3 [PMC free article] [PubMed] [CrossRef] [Google Scholar]150. Dangsuwan P, Manchana T. Blood transfusion reduction with intravenous iron in gynecologic cancer patients receiving chemotherapy. Gynecol Oncol. (2010) 116:522–5. 10.1016/j.ygyno.2009.12.004 [PubMed] [CrossRef] [Google Scholar]151. Hedenus M, Karlsson T, Ludwig H, Rzychon B, Felder M, Roubert B, et al. . Intravenous iron alone resolves anemia in patients with functional iron deficiency and lymphoid malignancies undergoing chemotherapy. Med Oncol. (2014) 31:302. 10.1007/s12032-014-0302-3 [PMC free article] [PubMed] [CrossRef] [Google Scholar]152. Steinmetz T, Tschechne B, Harlin O, Klement B, Franzem M, Wamhoff J, et al. . Clinical experience with ferric carboxymaltose in the treatment of cancer- and chemotherapy-associated anaemia. Ann Oncol. (2013) 24:475–82. 10.1093/annonc/mds338 [PMC free article] [PubMed] [CrossRef] [Google Scholar]153. Kim YT, Kim SW, Yoon BS, Cho HJ, Nahm EJ, Kim SH, et al. . Effect of intravenously administered iron sucrose on the prevention of anemia in the cervical cancer patients treated with concurrent chemoradiotherapy. Gynecol Oncol. (2007) 105:199–204. 10.1016/j.ygyno.2006.11.014 [PubMed] [CrossRef] [Google Scholar]154. Abdel-Razeq H, Abbasi S, Saadi I, Jaber R, Abdelelah H. Intravenous iron monotherapy for the treatment of non-iron-deficiency anemia in cancer patients undergoing chemotherapy: a pilot study. Drug Des Dev Ther. (2013) 7:939–44. 10.2147/DDDT.S45674 [PMC free article] [PubMed] [CrossRef] [Google Scholar]155. Birgegård G, Henry D, Glaspy J, Chopra R, Thomsen LL, Auerbach M. A randomized noninferiority trial of intravenous iron isomaltoside versus oral iron sulfate in patients with nonmyeloid malignancies and anemia receiving chemotherapy: the PROFOUND trial. Pharmacotherapy. (2016) 36:402–14. 10.1002/phar.1729 [PMC free article] [PubMed] [CrossRef] [Google Scholar]156. Vadhan-Raj S, Dahl NV, Bernard K, Li Z, Strauss WE. Efficacy and safety of IV ferumoxytol for iron deficiency anemia in patients with cancer. J Blood Med. (2017) 8:199–209. 10.2147/JBM.S138474 [PMC free article] [PubMed] [CrossRef] [Google Scholar]157. Verhaeghe L, Bruyneel L, Stragier E, Ferrante M, Dierickx D, Prenen H. The effectiveness of intravenous iron for iron deficiency anemia in gastrointestinal cancer patients: a retrospective study. Ann Gastroenterol. (2017) 30:654–63. 10.20524/aog.2017.0189 [PMC free article] [PubMed] [CrossRef] [Google Scholar]158. Keeler BD, Simpson JA, Ng S, Tselepis C, Iqbal T, Brookes MJ, et al. . The feasibility and clinical efficacy of intravenous iron administration for preoperative anaemia in patients with colorectal cancer. Colorectal Dis. (2014) 16:794–800. 10.1111/codi.12683 [PubMed] [CrossRef] [Google Scholar]159. Calleja JL, Delgado S, del Val A, Hervás A, Larraona JL, Terán Á, et al. . Ferric carboxymaltose reduces transfusions and hospital stay in patients with colon cancer and anemia. Int J Colorectal Dis. (2016) 31:543–51. 10.1007/s00384-015-2461-x [PMC free article] [PubMed] [CrossRef] [Google Scholar]160. Kam PM, Chu CW, Chan EM, Liu OL, Kwok KH. Use of intravenous iron therapy in colorectal cancer patient with iron deficiency anemia: a propensity-score matched study. Int J Colorectal Dis. (2020) 35:521–7. 10.1007/s00384-020-03508-y [PubMed] [CrossRef] [Google Scholar]161. Borstlap WA, Stellingwerf ME, Moolla Z, Musters GD, Buskens CJ, Tanis PJ, et al. . Iron therapy for the treatment of preoperative anaemia in patients with colorectal carcinoma: a systematic review. Colorectal Dis. (2015) 17:1044–54. 10.1111/codi.13110 [PubMed] [CrossRef] [Google Scholar]162. Keeler BD, Simpson JA, Ng O, Padmanabhan H, Brookes MJ, Acheson AG. Randomized clinical trial of preoperative oral versus intravenous iron in anaemic patients with colorectal cancer. Br J Surg. (2017) 104:214–21. 10.1002/bjs.10328 [PubMed] [CrossRef] [Google Scholar]163. Laso-Morales M, Jericó C, Gómez-Ramírez S, Castellví J, Viso L, Roig-Martínez I, et al. . Preoperative management of colorectal cancer-induced iron deficiency anemia in clinical practice: data from a large observational cohort. Transfusion. (2017) 57:3040–8. 10.1111/trf.14278 [PubMed] [CrossRef] [Google Scholar]164. Dickson EA, Keeler BD, Ng O, Kumar A, Brookes MJ, Acheson AG, et al. . Preoperative intravenous iron therapy and survival after colorectal cancer surgery: long-term results from the IVICA randomised controlled trial. Colorectal Dis. (2020) 22:2018–27. 10.1111/codi.15342 [PubMed] [CrossRef] [Google Scholar]165. Torti SV, Torti FM. Iron and cancer: more ore to be mined. Nat Rev Cancer. (2013) 13:342–55. 10.1038/nrc3495 [PMC free article] [PubMed] [CrossRef] [Google Scholar]166. Manz DH, Blanchette NL, Paul BT, Torti FM, Torti SV. Iron and cancer: recent insights. Ann N Y Acad Sci. (2016) 1368:149–61. 10.1111/nyas.13008 [PMC free article] [PubMed] [CrossRef] [Google Scholar]167. Gilreath JA, Stenehjem DD, Rodgers GM. Total dose iron dextran infusion in cancer patients: is it SaFe2+? J Nat Compr Canc Netw. (2012) 10:669–76. 10.6004/jnccn.2012.0066 [PubMed] [CrossRef] [Google Scholar]168. Wilson MJ, Harlaar JJ, Jeekel J, Schipperus M, Zwaginga JJ. Iron therapy as treatment of anemia: a potentially detrimental and hazardous strategy in colorectal cancer patients. Med Hypotheses. (2018) 110:110–3. 10.1016/j.mehy.2017.12.011 [PubMed] [CrossRef] [Google Scholar]169. Beguin Y, Aapro M, Ludwig H, Mizzen L, Osterborg A. Epidemiological and nonclinical studies investigating effects of iron in carcinogenesis–a critical review. Crit Rev Oncol Hematol. (2014) 89:1–15. 10.1016/j.critrevonc.2013.10.008 [PubMed] [CrossRef] [Google Scholar]170. Seril DN, Liao J, Ho KL, Warsi A, Yang CS, Yang GY. Dietary iron supplementation enhances DSS-induced colitis and associated colorectal carcinoma development in mice. Digest Dis Sci. (2002) 47:1266–78. 10.1023/A:1015362228659 [PubMed] [CrossRef] [Google Scholar]171. Ilsley JN, Belinsky GS, Guda K, Zhang Q, Huang X, Blumberg JB, et al. . Dietary iron promotes azoxymethane-induced colon tumors in mice. Nutr Cancer. (2004) 49:162–9. 10.1207/s15327914nc4902_7 [PubMed] [CrossRef] [Google Scholar]172. Seril DN, Liao J, Yang CS, Yang GY. Systemic iron supplementation replenishes iron stores without enhancing colon carcinogenesis in murine models of ulcerative colitis: comparison with iron-enriched diet. Digest Dis Sci. (2005) 50:696–707. 10.1007/s10620-005-2560-6 [PubMed] [CrossRef] [Google Scholar]173. Chua AC, Klopcic B, Lawrance IC, Olynyk JK, Trinder D. Iron: an emerging factor in colorectal carcinogenesis. World J Gastroenterol. (2010) 16:663–72. 10.3748/wjg.v16.i6.663 [PMC free article] [PubMed] [CrossRef] [Google Scholar]174. Radulescu S, Brookes MJ, Salgueiro P, Ridgway RA, McGhee E, Anderson K, et al. . Luminal iron levels govern intestinal tumorigenesis after Apc loss in vivo. Cell Rep. (2016) 17:2805–7. 10.1016/j.celrep.2016.10.028 [PubMed] [CrossRef] [Google Scholar]175. Jaspers A, Baron F, Servais S, Lejeune M, Willems É, Seidel L, et al. . Erythropoietin therapy after allogeneic hematopoietic cell transplantation has no impact on long-term survival. Am J Hematol. (2015) 90:E197–9. 10.1002/ajh.24100 [PubMed] [CrossRef] [Google Scholar]176. Wilson MJ, Dekker JWT, Buettner S, Harlaar JJ, Jeekel J, Schipperus M, et al. . The effect of intravenous iron therapy on long-term survival in anaemic colorectal cancer patients: Results from a matched cohort study. Surg Oncol. (2018) 27:192–9. 10.1016/j.suronc.2018.03.005 [PubMed] [CrossRef] [Google Scholar]177. Nairz M, Dichtl S, Schroll A, Haschka D, Tymoszuk P, Theurl I, et al. . Iron and innate antimicrobial immunity-depriving the pathogen, defending the host. J Trace Elem Med Biol. (2018) 48:118–33. 10.1016/j.jtemb.2018.03.007 [PubMed] [CrossRef] [Google Scholar]178. Auerbach M, Silberstein PT, Webb RT, Averyanova S, Ciuleanu TE, Shao J, et al. . Darbepoetin alfa 300 or 500 μg once every 3 weeks with or without intravenous iron in patients with chemotherapy-induced anemia. Am J Hematol. (2010) 85:655–63. 10.1002/ajh.21779 [PubMed] [CrossRef] [Google Scholar]179. Bastit L, Vandebroek A, Altintas S, Gaede B, Pintér T, Suto TS, et al. . Randomized, multicenter, controlled trial comparing the efficacy and safety of darbepoetin alpha administered every 3 weeks with or without intravenous iron in patients with chemotherapy-induced anemia. J Clin Oncol. (2008) 26:1611–8. 10.1200/JCO.2006.10.4620 [PubMed] [CrossRef] [Google Scholar]180. Hedenus M, Birgegård G, Näsman P, Ahlberg L, Karlsson T, Lauri B, et al. . Addition of intravenous iron to epoetin beta increases hemoglobin response and decreases epoetin dose requirement in anemic patients with lymphoproliferative malignancies: a randomized multicenter study. Leukemia. (2007) 21:627–32. 10.1038/sj.leu.2404562 [PubMed] [CrossRef] [Google Scholar]